พญ. ฮูดัยบ๊ะห์ มูหามัด
พญ. ฮูดัยบ๊ะห์ มูหามัด
สาขาวิชาโรคติดเชื้อ ภาควิชากุมารเวชศาสตร์
คณะแพทยศาสตร์ศิริราชพยาบาล
 รศ.พญ. เกษวดี ลาภพระ
รศ.พญ. เกษวดี ลาภพระ
สาขาวิชาโรคติดเชื้อ ภาควิชากุมารเวชศาสตร์
คณะแพทยศาสตร์ศิริราชพยาบาล
โรคหนองใน (Gonorrhea) เป็นโรคติดต่อทางเพศสัมพันธ์ที่ยังคงเป็นปัญหาสาธารณสุขสำคัญในระดับโลก องค์การอนามัยโลก (WHO) ประมาณการว่าในปี พ.ศ. 2563 (ค.ศ. 2020) มีผู้ติดเชื้อรายใหม่ทั่วโลกประมาณ 82.4 ล้านราย ในประชากรอายุ 15 – 49 ปี โดยมีอัตราอุบัติการณ์เท่ากับ 23 ราย ต่อประชากร 1,000 คนในเพศชาย และ 19 ราย ต่อประชากร 1,000 คนในเพศหญิง(1) สำหรับประเทศไทย ในปี พ.ศ. 2568 มีรายงานผู้ติดเชื้อหนองในรายใหม่จำนวน 17,436 ราย โดยอัตราการติดเชื้อสูงสุดในกลุ่มอายุ 15 – 29 ปี(2) ทั้งนี้ ผู้ติดเชื้อหนองในมีความเสี่ยงต่อการติดเชื้อโรคติดต่อทางเพศสัมพันธ์อื่นร่วมด้วย เช่น เอชไอวี (HIV) และซิฟิลิส (syphilis) ซึ่งส่งผลให้เกิดภาระด้านสาธารณสุขในหลายประเทศทั่วโลก
แนวทางการรักษาการติดเชื้อหนองใน (Gonococcal infections) ตามคำแนะนำของ WHO ฉบับปรับปรุงปี ค.ศ. 2023(3) สำหรับการติดเชื้อหนองในบริเวณอวัยวะสืบพันธุ์ ทวารหนัก และ/หรือคอหอยในวัยรุ่นและผู้ใหญ่ รวมถึงหญิงตั้งครรภ์ มีรายละเอียดดังนี้
การรักษาหลัก: Ceftriaxone ขนาด 1 กรัม ฉีดเข้ากล้ามเนื้อ (IM) ครั้งเดียว
- ในกรณีที่ไม่สามารถใช้ ceftriaxone ได้ หรือผู้ป่วยปฏิเสธการฉีดยา : ให้ Cefixime ขนาด 800 มิลลิกรัม รับประทานครั้งเดียว และควรทำการตรวจยืนยันการหายของเชื้อ (test of cure)
- ในกรณีที่ไม่สามารถทำ test of cure ได้ หรือมีการติดเชื้อที่คอหอย (ยืนยันหรือสงสัย) : ให้ Cefixime ขนาด 800 มิลลิกรัม รับประทานครั้งเดียว ร่วมกับ Azithromycin ขนาด 2 กรัม รับประทานครั้งเดียว
- ในกรณีที่มีความกังวลเรื่องการดื้อยา การแพ้ยา หรือไม่สามารถใช้ยากลุ่ม cephalosporins
- Spectinomycin ขนาด 2 กรัม ฉีดเข้ากล้ามเนื้อครั้งเดียว ร่วมกับ Azithromycin ขนาด 2 กรัม รับประทานครั้งเดียว
- Gentamicin ขนาด 240 มิลลิกรัม ฉีดเข้ากล้ามเนื้อครั้งเดียว ร่วมกับ Azithromycin ขนาด 2 กรัม รับประทานครั้งเดียว
- Azithromycin ขนาด 2 กรัม อาจทำให้เกิดอาการไม่พึงประสงค์ทางระบบทางเดินอาหาร โดยเฉพาะเมื่อรับประทานขณะท้องว่าง อาจพิจารณาแบ่งขนาดยาเป็น 1 กรัม ทุก 6 – 12 ชั่วโมง เพื่อลดอาการดังกล่าว
- ควรให้คำแนะนำผู้ป่วยเกี่ยวกับการงดมีเพศสัมพันธ์ การใช้ถุงยางอนามัยสม่ำเสมอและรักษาคู่นอน
- ในหญิงตั้งครรภ์ ควรติดตามอาการไม่พึงประสงค์อย่างใกล้ชิด เช่น ภาวะแพ้ยารุนแรง (anaphylactic shock) การคลอดก่อนกำหนด (preterm labor) และ ภาวะถุงน้ำคร่ำแตกก่อนกำหนด (premature rupture of membrane) เป็นต้น
หากรักษาที่ให้ไปก่อนหน้านั้นล้มเหลว โดยมีหลักฐานจากอาการที่ยังคงอยู่อย่างต่อเนื่อง หรือผลตรวจยืนยันการติดเชื้อหนองในยังคงเป็นบวก ควรพิจารณาความเป็นไปได้ของการติดเชื้อซ้ำ (reinfection) หรือการดื้อยาต้านจุลชีพ (antimicrobial resistance) โดยมีข้อแนะนำดังต่อไปนี้
- กรณีการรักษาล้มเหลวหลังได้รับสูตรยาที่ไม่เป็นไปตามแนวทางที่แนะนำ แนะนำให้ทำการรักษาซ้ำโดยใช้สูตรยามาตรฐานตามแนวทางที่แนะนำ
- กรณีสงสัยการติดเชื้อเชื้อใหม่ (reinfection) แนะนำให้ทำการรักษาซ้ำโดยใช้สูตรยาที่แนะนำ พร้อมทั้งเน้นย้ำการงดการมีเพศสัมพันธ์ การใช้ถุงยางอนามัยอย่างสม่ำเสมอ และการรักษาคู่นอนทุกราย
- กรณีการรักษาล้มเหลวและมีผลการทดสอบความไวต่อยาต้านจุลชีพ (antimicrobial susceptibility testing)
แนะนำให้เลือกสูตรการรักษาซ้ำโดยพิจารณาตามผลความไวของเชื้อ - กรณีการรักษาล้มเหลวหลังได้รับสูตรยาที่แนะนำ และประเมินแล้วว่าไม่น่าจะเป็นการติดเชื้อซ้ำ แนะนำให้รักษาซ้ำด้วยสูตรยาที่แตกต่างจากเดิม โดยเลือกหนึ่งในทางเลือกต่อไปนี้ และควรทำการตรวจยืนยันการหายของเชื้อ (test of cure)
- Ceftriaxone ขนาด 1 กรัม ฉีดเข้ากล้ามเนื้อครั้งเดียว ร่วมกับ Azithromycin ขนาด 2 กรัม รับประทานครั้งเดียว
(ให้ใช้เฉพาะในกรณีที่ยังไม่เคยให้ ceftriaxone มาก่อน) - Spectinomycin ขนาด 2 กรัม ฉีดเข้ากล้ามเนื้อครั้งเดียว ร่วมกับ Azithromycin ขนาด 2 กรัม รับประทานครั้งเดียวGentamicin ขนาด 240 มิลลิกรัม ฉีดเข้ากล้ามเนื้อครั้งเดียว ร่วมกับ Azithromycin ขนาด 2 กรัม รับประทานครั้งเดียว
- Ceftriaxone ขนาด 1 กรัม ฉีดเข้ากล้ามเนื้อครั้งเดียว ร่วมกับ Azithromycin ขนาด 2 กรัม รับประทานครั้งเดียว
เชื้อ Neisseria gonorrhoeae ที่ดื้อต่อยาปฏิชีวนะกำลังเป็นปัญหาสาธารณสุขที่สำคัญทั่วโลก แนวทางใหม่ในการรับมือกับปัญหานี้คือการพัฒนาเทคนิคการตรวจระดับโมเลกุล เพื่อทำนายความไวต่อยาปฏิชีวนะ และช่วยให้สามารถเลือกการรักษาเฉพาะรายได้อย่างเหมาะสม (Resistance Guided Therapy) (4)
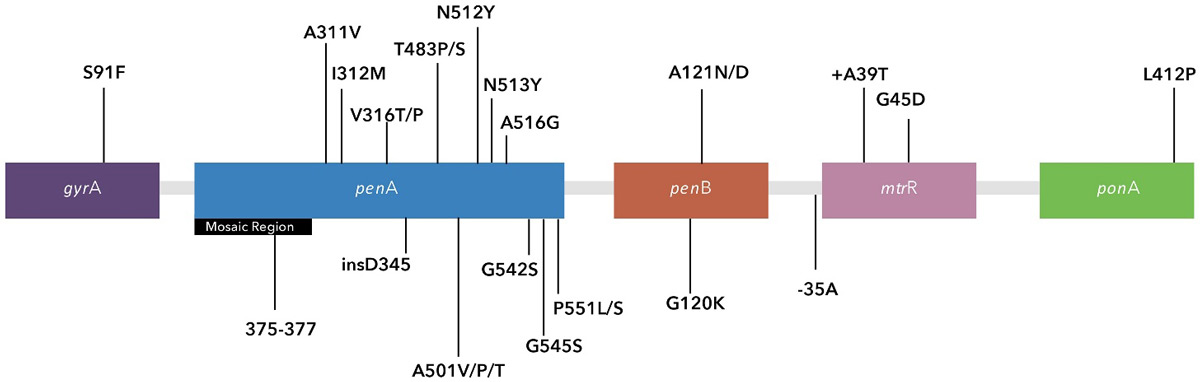
รูปที่ 1 การกลายพันธุ์ของเชื้อ Neisseria gonorrhoeae ที่เกี่ยวข้องกับการลดความไวต่อยา ciprofloxacin, cefixime และ ceftriaxone
(อ้างอิงจากเอกสารหมายเลข 4)
Resistance-Guided Therapy สำหรับยา ciprofloxacin
- Ciprofloxacin ออกฤทธิ์ยับยั้งเอนไซม์ DNA-gyrase และ topoisomerase IV
- การดื้อยามักเกิดจากการกลายพันธุ์ในยีน gyrA (ตำแหน่ง S91) และ parC หากไม่พบการกลายพันธุ์ที่ codon 91 ของ gyrA สามารถทำนายได้ค่อนข้างแม่นยำว่าเชื้อยังไวต่อยา ciprofloxacin
- ปัจจุบันพบอัตราการดื้อ ciprofloxacin เพิ่มสูงขึ้นทั่วโลก (หลายประเทศมากกว่า 30 – 70%) จึง ไม่เหมาะสมสำหรับการให้ยาโดยไม่ตรวจยืนยัน
- ในกรณีที่ยืนยันว่าเชื้อยังไวต่อ ciprofloxacin สามารถให้ยาในรูปแบบรับประทานครั้งเดียว แทนการฉีด ceftriaxone ได้อย่างปลอดภัย โดยการศึกษาขนาดใหญ่รายงานอัตราความสำเร็จของการรักษาสูงถึง 100% ด้วยเหตุนี้ แนวทางเวชปฏิบัติในสหรัฐอเมริกา สหราชอาณาจักร และออสเตรเลีย จึงอนุญาตให้ใช้ ciprofloxacin เฉพาะในกรณีที่ ยืนยันแล้วว่าเชื้อยังไวต่อยา
Resistance-Guided Therapy สำหรับยากลุ่ม Cephalosporins
กลไกการดื้อยากลุ่ม cephalosporins ของเชื้อ Neisseria gonorrhoeae มีความซับซ้อนและหลากหลายมากกว่ายา ciprofloxacin อย่างมีนัยสำคัญ โดยมียีนหลักที่เกี่ยวข้องกับการดื้อยาจำนวน 4 ยีน ได้แก่ penA, penB, mtrR และ ponA
- penA: encode penicillin-binding protein 2 (PBP2) พบว่าการกลายพันธุ์ในตำแหน่งกรดอะมิโนได้มากถึง 83 ตำแหน่ง มีความสัมพันธ์กับการลดความไวต่อยา ceftriaxone โดยภายในยีน penA แบ่งเป็น
- mosaic region ซึ่งเกิดจากการแลกเปลี่ยนสารพันธุกรรมกับ Neisseria ชนิดไม่ก่อโรค
- non-mosaic region ซึ่งจำเพาะต่อ gonorrhoeae
- penB: encode PorB (outer membrane porin) ทำให้การซึมผ่านของยาปฏิชีวนะเข้าสู่เยื่อหุ้มเซลล์ลดลง
- mtrR: ทำให้ระบบ efflux pump ทำงานเพิ่มขึ้น
- ponA: encode penicillin-binding protein 1 (PBP1) ซึ่งมีบทบาทต่อการดื้อยาในระดับรองลงมา
การดื้อยา cefixime มีความสัมพันธ์อย่างใกล้ชิดกับการกลายพันธุ์สำคัญในยีน penA โดยเฉพาะ mosaic penA gene (เช่น penA34) รวมถึงตำแหน่งจำเพาะใน non-mosaic penA region ขณะที่การดื้อยา ceftriaxone มีความซับซ้อนมากกว่า เนื่องจากเกี่ยวข้องกับการกลายพันธุ์ในหลายยีน ได้แก่ penA, ponA, penB และ mtr ซึ่งส่งผลต่อโครงสร้างเป้าหมายยา การซึมผ่านของยา และการขับยาออกจากเซลล์ ทั้งนี้ ความแม่นยำในการทำนายการลดความไวต่อยาจากตัวบ่งชี้ระดับโมเลกุลขึ้นอยู่กับสายพันธุ์เด่นและบริบททางระบาดวิทยาในแต่ละภูมิศาสตร์ เนื่องจากมีกลไกการดื้อยาหลายรูปแบบและหลายตำแหน่งการกลายพันธุ์ร่วมกัน การทำนายลักษณะการดื้อยา (phenotype) ของยากลุ่ม cephalosporins จึงเป็นความท้าทายอย่างมาก
รายงานการดื้อยารักษาหลักของโรคหนองในเพิ่มมากขึ้นในหลายประเทศ องค์การอนามัยโลก (WHO) จึงได้ดำเนินแผนปฏิบัติการเพื่อควบคุมการแพร่กระจายและลดผลกระทบของการดื้อยาต้านจุลชีพในเชื้อ Neisseria gonorrhoeae โดยมุ่งสนับสนุนมาตรการด้านการเฝ้าระวัง การควบคุม และชะลอการแพร่กระจายของเชื้อหนองในดื้อยาหลายขนาน ควบคู่กับการวิจัยและการพัฒนายาต้านจุลชีพรุ่นใหม่อย่างต่อเนื่อง
ในปี 2568 องค์การอาหารและยาสหรัฐอเมริกา (U.S. Food and Drug Administration; FDA) ได้ประกาศอนุมัติยาปฏิชีวนะชนิดรับประทานใหม่ 2 ชนิดสำหรับการรักษาโรคหนองใน ซึ่งนับเป็นความก้าวหน้าทางการรักษาที่สำคัญในรอบหลายทศวรรษ ท่ามกลางสถานการณ์การดื้อต่อยาที่ทวีความรุนแรง ยาทั้งสองชนิด ได้แก่(5)
- Zoliflodacin (ชื่อการค้า Nuzolvence) : ยาเม็ดรับประทานครั้งเดียวสำหรับการรักษา gonorrhea แบบไม่ซับซ้อนในระบบสืบพันธุ์และทางเดินปัสสาวะ ในผู้ใหญ่และวัยรุ่นอายุ ≥12 ปี และน้ำหนัก ≥35 กิโลกรัม
- Gepotidacin (ชื่อการค้า Blujepa) : ยาเม็ดรับประทานที่ขยายข้อบ่งใช้สำหรับการรักษา gonorrhea แบบไม่ซับซ้อนในผู้ที่มีตัวเลือกการรักษาจำกัด ในผู้ใหญ่และวัยรุ่นอายุ ≥12 ปี และน้ำหนัก ≥45 กิโลกรัมโดยก่อนหน้านี้ได้รับการอนุมัติสำหรับการรักษาการติดเชื้อทางเดินปัสสาวะไม่ซับซ้อนแล้ว
ตารางที่ 1 การเปรียบเทียบยา Zoliflodacin และ Gepotidacin สำหรับการรักษาการติดเชื้อ Neisseria gonorrhea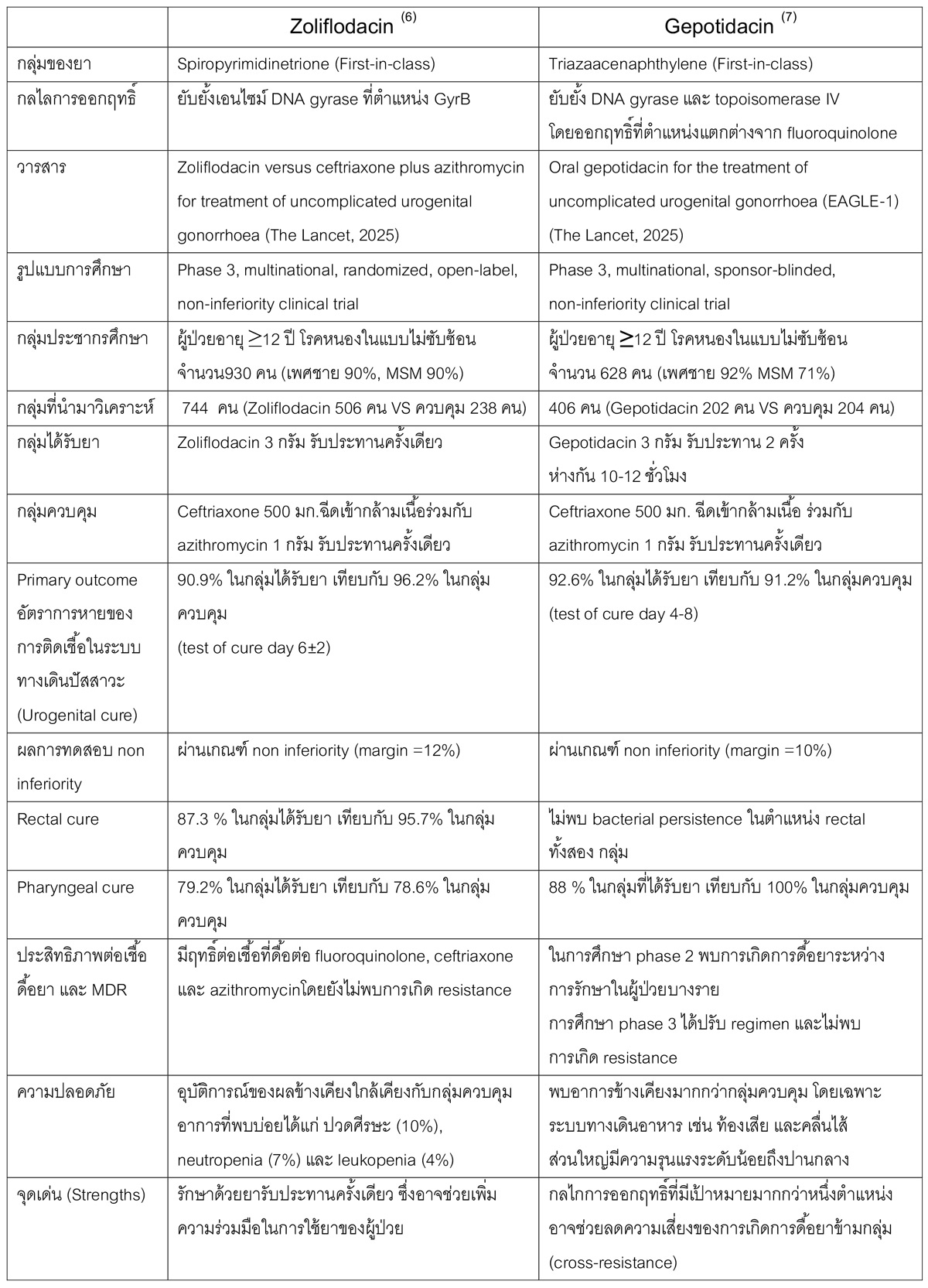
การรักษาหรือมาตรการอื่นที่มีผลต่อการลดความเสี่ยงการติดเชื้อ Neisseria gonorrhoeae
- วัคซีน 4CMenB
วัคซีน meningococcal group B ชนิด outer membrane vesicle (OMV) ซึ่งพัฒนาขึ้นเพื่อป้องกันการติดเชื้อ Neisseria meningitidis อาจให้ผลในการป้องกันการติดเชื้อ Neisseria gonorrhoeae แบบข้ามสายพันธุ์ (cross-protection) เนื่องจากเชื้อทั้งสองชนิดมีความคล้ายคลึงกันสูงทั้งในระดับพันธุกรรมและแอนติเจน (ประมาณ 80 – 90%) วัคซีนชนิด OMV ซึ่งประกอบด้วยโปรตีนจากเยื่อหุ้มชั้นนอกของ N. meningitidis จึงอาจกระตุ้นการตอบสนองทางภูมิคุ้มกันต่อโครงสร้างที่มีความคล้ายคลึงกันบนผิวของ N. gonorrhoeae ส่งผลให้ลดความเสี่ยงต่อการเกิดโรคหนองในได้
จากการศึกษาแบบ systematic review และ meta-analysis ที่รวบรวมข้อมูลจากงานวิจัยเชิงสังเกตหลายการศึกษา พบว่า วัคซีน meningococcal B vaccine ชนิด OMV-based (เช่น 4CMenB หรือ MeNZB) มีประสิทธิผลในการลดความเสี่ยงต่อการติดเชื้อ N. gonorrhoeae ประมาณร้อยละ 30 – 40 เมื่อเทียบกับผู้ที่ไม่ได้รับวัคซีน (8) นอกจากนี้ การศึกษาเชิงสังเกตแบบ case-control study หลังจากเริ่มใช้วัคซีน 4CMenB เป็นระยะเวลา 4 ปี ยังรายงานว่า วัคซีนดังกล่าวมีประสิทธิผลในระดับปานกลางในการลดความเสี่ยงต่อการติดเชื้อหนองใน คิดเป็นร้อยละ 36.5 (9) - Doxycycline Postexposure Prophylaxis (Doxy-PEP)
บทความในวารสาร JAMA Internal Medicine ปี ค.ศ. 2025 (10) ศึกษาผลของการใช้ doxycycline เป็นการป้องกันหลังการสัมผัสเชื้อ (doxycycline post-exposure prophylaxis;doxy-PEP) ในกลุ่มผู้ที่ได้รับการป้องกันการติดเชื้อเอชไอวีแบบก่อนการสัมผัสเชื้อ (HIV pre-exposure prophylaxis; HIV PrEP) เพื่อประเมินความสัมพันธ์ระหว่างการใช้ doxy-PEP กับอุบัติการณ์ของโรคติดต่อทางเพศสัมพันธ์ที่มีสาเหตุจากเชื้อแบคทีเรีย
- การติดเชื้อ Chlamydia trachomatis ลดลงร้อยละ 79
- การติดเชื้อซิฟิลิส (Treponema pallidum) ลดลงร้อยละ 80
- ขณะที่การติดเชื้อหนองในแท้ (Neisseria gonorrhoeae) ลดลงเพียงร้อยละ 12
ประสิทธิผลที่ค่อนข้างจำกัดของ doxy-PEP ต่อการลดการติดเชื้อหนองใน อาจสอดคล้องกับข้อมูลที่มีอยู่เดิมซึ่งแสดงให้เห็นว่าเชื้อดังกล่าวมีอัตราการดื้อต่อยาปฏิชีวนะในกลุ่ม tetracycline อยู่ในระดับสูงเมื่อเทียบกับเชื้อแบคทีเรียก่อโรคติดต่อทางเพศสัมพันธ์ชนิดอื่น
-
- World Health Organization (WHO). Multi-drug resistant gonorrhea: fact sheet [Internet]. 2025 Oct 22 [cited 2025 Dec 27]. Available from: https://www.who.int/news-room/fact-sheets/detail/multi-drug-resistant-gonorrhoea
- Department of Disease Control, Ministry of Public Health. Notifiable communicable diseases weekly report dashboard (Gonorrhea) [Internet]. Bangkok: DDC; 2025 [cited 2025 Dec 27]. Available from:https://dvis3.ddc.moph.go.th/t/DDC_CENTER_DOE/views/_Weekly/sheet13
- World Health Organization. Updated recommendations for the treatment of Neisseria gonorrhoeae, Chlamydia trachomatis and Treponema pallidum and new recommendations on syphilis testing and partner services. Geneva: World Health Organization; 2024. Licence: CC BY-NC-SA 3.0 IGO. ISBN: 978-92-4-009076-7
- Lao-Tzu Allan-Blitz, Paul C Adamson, Jeffrey D Klausner, Resistance-Guided Therapy for Neisseria gonorrhoeae, Clinical Infectious Diseases, Volume 75, Issue 9, 1 November 2022, Pages 1655–1660, https://doi.org/10.1093/cid/ciac371
- S. Food and Drug Administration. (2025, December 12). FDA approves two oral therapies to treat gonorrhea: Approvals are for uncomplicated urogenital gonorrhea (Press release). U.S. Department of Health and Human Services. https://www.fda.gov/news-events/press-announcements/fda-approves-two-oral-therapies-treat-gonorrhea
- Luckey A, Balasegaram M, Barbee LA, et al. Zoliflodacin versus ceftriaxone plus azithromycin for treatment of uncomplicated urogenital gonorrhoea: an international, randomised, controlled, open-label, phase 3, non-inferiority clinical trial. Lancet. Published online December 11, 2025. doi:10.1016/S0140-6736(25)01953-1
- Ross JDC, Wilson J, Workowski KA, et al. Oral gepotidacin for the treatment of uncomplicated urogenital gonorrhoea (EAGLE-1): a phase 3 randomised, open-label, non-inferiority, multicentre study. Lancet. 2025;405(10489):1608-1620. doi:10.1016/S0140-6736(25)00628-2
- Wang B, Mohammed H, Andraweera P, McMillan M, Marshall H. Vaccine effectiveness and impact of meningococcal vaccines against gonococcal infections: A systematic review and meta-analysis. J Infect. 2024;89(3):106225. doi:10.1016/j.jinf.2024.106225
- Wang et al. Long-term 4CMenB Vaccine Effectiveness Against Gonococcal Infection at Four Years Post–Program Implementation:Observational Case–Control Study, Open Forum Infectious Diseases, volume 12, issue 1, January 2025.
- Traeger MW, Leyden WA, Volk JE, et al. Doxycycline Postexposure Prophylaxis and Bacterial Sexually Transmitted Infections Among Individuals Using HIV Preexposure Prophylaxis. JAMA Intern Med. 2025;185(3):273-281. doi:10.1001/jamainternmed.2024.7186