พญ. ปาณิสรา ลักขณา
พญ. ปาณิสรา ลักขณา
หน่วยโรคติดเชื้อ ภาควิชากุมารเวชศาสตร์
คณะแพทยศาสตร์ศิริราชพยาบาล
 ผศ. พญ. สุพัตรา รุ่งไมตรี
ผศ. พญ. สุพัตรา รุ่งไมตรี
สาขาวิชาโรคติดเชื้อ ภาควิชากุมารเวชศาสตร์
คณะแพทยศาสตร์ศิริราชพยาบาล
โรคติดเชื้อ cytomegalovirus (CMV disease) เป็นโรคติดเชื้อฉวยโอกาสที่สำคัญในผู้ป่วยที่มีภาวะภูมิคุ้มกันต่ำ ได้แก่ ผู้ป่วยที่ได้รับยากดภูมิภายหลังการปลูกถ่ายอวัยวะ (solid organ transplantation, SOT) หรือเซลล์ต้นกำเนิดเม็ดเลือด (hematopoietic stem cell transplantation, HSCT) CMV disease ทำให้เกิดอาการที่รุนแรง เช่น ปอดอักเสบ ลำไส้อักเสบ การเกิดปฏิกิริยา graft versus host disease (GvHD) และอาจมีความรุนแรงจนถึงขั้นเสียชีวิตได้ การป้องกัน CMV disease สามารถทำได้ 2 วิธี คือ การให้ยาป้องกัน (prophylaxis) และ การใช้ยารักษาต่อเมื่อมีการพบค่าทางห้องปฏิบัติการที่บ่งชี้ว่ามีการติดเชื้อ (pre-emptive therapy) ที่ผ่านมาการให้ยาต้านไวรัสเพื่อป้องกัน ได้แก่ ganciclovir, valganciclovir พบว่าสามารถลดอุบัติการณ์ของโรคติดเชื้อ CMV ได้ แต่ไม่ลดอัตราการเสียชีวิต และพบอาการข้างเคียงที่สำคัญคือ การกดไขกระดูก ซึ่งเพิ่มความเสี่ยงของการติดเชื้อแบคทีเรีย และเชื้อรา ส่วนใหญ่จึงนิยมวิธี pre-emptive therapy
- แนะนำให้ตรวจ CMV serostatus ตั้งแต่ช่วงวินิจฉัยโรคหลัก และตรวจซ้ำก่อนการปลูกถ่าย HCT เนื่องจาก CMV serostatus เป็นปัจจัยทำนายความเสี่ยงที่สำคัญที่สุดของการเกิด CMV reactivation หลังการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือด และส่งผลโดยตรงต่อการวางแผน prophylaxis และการติดตามภายหลังการปลูกถ่าย
- ยา letermovir แนะนำให้เป็น first-line strategy สำหรับ primary prophylaxis ในผู้ป่วยผู้ใหญ่ที่มี CMV-seropositive และได้รับ allogeneic HCT เนื่องจากสามารถลดการเกิด CMV reactivation ได้อย่างมีนัยสำคัญ ลดการเกิด CMV disease และมีข้อมูลสนับสนุนว่าช่วยลด mortality และภาวะแทรกซ้อนอื่น เช่น graft-versus-host disease (GVHD) นอกจากนี้ letermovir ยังมีความปลอดภัยสูง และไม่กดการทำงานของไขกระดูก
- การใช้ letermovir ในผู้ป่วยเด็ก แม้ว่าหลักฐานในผู้ป่วยเด็กยังมีจำกัดเมื่อเทียบกับผู้ใหญ่ แต่แนวทาง ECIL-10 แนะนำให้ พิจารณาใช้ letermovir ในเด็กที่มีความเสี่ยงสูง โดยเฉพาะในกลุ่มที่มี CMV-seropositive และได้รับ allogeneic HCT เนื่องจากข้อมูลปัจจุบันชี้ว่า letermovir มีความปลอดภัยดี และมีแนวโน้มช่วยลดการเกิด CMV infection ได้ โดยคำแนะนำอยู่ในระดับ A-II ซึ่งหมายถึงมีหลักฐานสนับสนุนที่ดีจากการศึกษาเชิงคลินิก (non-randomized studies) ที่มีความน่าเชื่อถือเพียงพอสำหรับการนำไปใช้ในเวชปฏิบัติ
พยาธิสรีรวิทยา CMV วงจรการเพิ่มจำนวน และกลไกการออกฤทธิ์ของ letermovir2
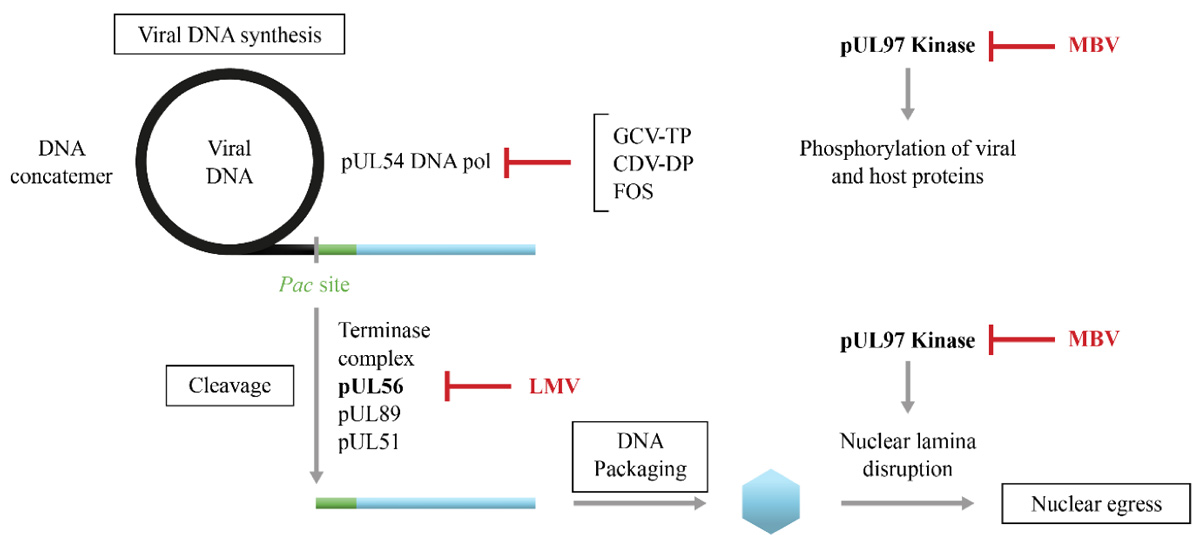
กระบวนการเพิ่มจำนวนของเชื้อ CMV เริ่มต้นจากการเข้าสู่เซลล์เจ้าบ้าน (viral entry) ผ่านกระบวนการ receptor-mediated endocytosis หลังจากนั้นสารพันธุกรรมของไวรัส (viral DNA) จะถูกลำเลียงเข้าสู่นิวเคลียส และเริ่มกระบวนการถอดรหัสและการจำลองสารพันธุกรรม (DNA replication) ส่งผลให้เกิดการสร้าง DNA ปริมาณมากในลักษณะสายยาวต่อเนื่องที่เรียกว่า concatemeric DNA
- UL56 ทำหน้าที่เป็น subunit หลักในการจดจำและจับ viral DNA และเป็นเป้าหมายสำคัญของยา
- UL89 มีบทบาทด้าน endonuclease activity ช่วยในการตัด DNA
ยา letermovir เป็นยาต้านไวรัสชนิดใหม่ที่ออกฤทธิ์โดยการยับยั้ง CMV terminase complex โดยเฉพาะที่โปรตีน UL56 และ UL89 ส่งผลให้กระบวนการ cleavage และ packaging ของ viral DNA ถูกยับยั้ง ทำให้ไวรัสไม่สามารถสร้างอนุภาคที่สมบูรณ์ได้ จุดเด่นของ letermovir คือการออกฤทธิ์ในระยะท้ายของวงจรไวรัส (late stage inhibition) ซึ่งแตกต่างจากยาต้านไวรัสแบบดั้งเดิม เช่น ganciclovir ที่ออกฤทธิ์ยับยั้ง DNA polymerase ในระยะ DNA replication ดังนั้น letermovir จึงมีความจำเพาะต่อ CMV สูง และมีผลกระทบต่อเซลล์ของร่างกายน้อย โดยเฉพาะ ไม่กดการทำงานของไขกระดูก (รูปที่ 1)
รูปที่ 1 แสดงกลไกการออกฤทธิ์ของยาต้าน Letermovir ต่อ Cytomegalovirus2
บทบาทของ letermovir ในการป้องกัน CMV หลังการปลูกถ่าย HCT1
การใช้ letermovir prophylaxis นับตั้งแต่เริ่มนำมาใช้ในปี ค.ศ. 2018 ได้กลายเป็นมาตรฐานในการป้องกัน clinically significant CMV infection (CS-CMVi) ในผู้ป่วยผู้ใหญ่ที่มี CMV seropositive และได้รับการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือดชนิด allogeneic HCT โดยการศึกษาหลัก (pivotal study) แสดงให้เห็นว่า letermovir ไม่เพียงช่วยลดความเสี่ยงของ CS-CMVi อย่างมีนัยสำคัญ แต่ยังสามารถลดอัตราการเสียชีวิตจากทุกสาเหตุ (all-cause mortality) ได้อีกด้วย3, 4
องค์การอาหารและยาของสหรัฐอเมริกา (US-FDA) ได้อนุมัติการใช้ยา letermovir พร้อมทั้งมีการปรับปรุงข้อมูลกำกับยาให้ครอบคลุม รูปแบบยาชนิดใหม่ (oral pellets) และขยายข้อบ่งใช้ไปยังผู้ป่วยเด็กที่ได้รับ HCT ซึ่งมีอายุตั้งแต่ 6 เดือนขึ้นไป และมีน้ำหนักอย่างน้อย 6 กิโลกรัม ซึ่งการขยายข้อบ่งใช้ดังกล่าวมาจากข้อมูลสนับสนุนทางเภสัชจลนศาสตร์ และข้อมูลด้านความปลอดภัย จากการศึกษาเชิงคลินิกระยะที่ 2b แบบ multicenter, open-label, single-arm study ซึ่งประเมินการใช้ยา letermovir ในผู้ป่วยเด็ก 65 ราย อายุระหว่าง 2 เดือนถึงน้อยกว่า 18 ปี5 โดยแบ่งออกเป็น 3 กลุ่มอายุ ได้แก่ 12 ปี ถึง <18 ปี, 2 ปี ถึง <12 ปี, และ 2 เดือน ถึง <2 ปี
ผลลัพธ์ด้านประสิทธิภาพพบว่า อัตราความล้มเหลวของการรักษา (treatment failure) เมื่อวิเคราะห์ด้วยวิธี non-completer = failure (NC=F) อยู่ที่ ร้อยละ 19.6 ในสัปดาห์ที่ 14 และ ร้อยละ 25.0 ในสัปดาห์ที่ 24 หลังการปลูกถ่าย อย่างไรก็ตาม เมื่อพิจารณาเฉพาะ CS-CMVi โดยใช้วิธี data as observed (DAO) พบอัตราที่ต่ำกว่า คือ ร้อยละ 8.2 และ ร้อยละ 12.5 ตามลำดับ และไม่พบการเกิด CMV end-organ disease ในผู้ป่วยที่ศึกษา โดยสรุป การใช้ letermovir ในผู้ป่วยเด็กที่ได้รับ allogenic-HCT และมี CMV seropositive (R+) สามารถให้ระดับยาใกล้เคียงกับผู้ใหญ่ มีประสิทธิภาพในการลด CS-CMVi และมีความปลอดภัยในระดับที่ยอมรับได้ ผลการศึกษานี้ยังสนับสนุนการใช้แบบจำลอง population pharmacokinetics (Pop PK) เพื่อกำหนดขนาดยาที่เหมาะสมในผู้ป่วยเด็ก5
การศึกษาโดย Chen et al. (2023)6 เป็นการศึกษาแบบ retrospective matched cohort study ในศูนย์เดียว โดยเปรียบเทียบผู้ป่วยเด็กที่ได้รับ letermovir (LTV) prophylaxis กับกลุ่มที่ไม่ได้รับการป้องกัน CMV ภายหลังได้รับ HCT จุดมุ่งหมายหลักของการศึกษา (primary endpoint) คือการเกิด clinically significant CMV DNAemia ซึ่งนิยามว่า มีค่า viral load >1,000 copies/mL หรือตรวจพบ CMV DNAemia ในระดับใดก็ตามที่นำไปสู่การเริ่ม pre-emptive therapy ผลการศึกษาพบว่า กลุ่มที่ได้รับ LTV มีอุบัติการณ์ของ clinically significant CMV DNAemia ภายใน 180 วันหลังปลูกถ่าย (D+180) ต่ำกว่ากลุ่มควบคุม (ร้อยละ 9.8 เทียบกับ ร้อยละ 17.0) แม้ว่าความแตกต่างจะไม่ถึงระดับนัยสำคัญทางสถิติ (p = 0.33) แต่แสดงถึงแนวโน้มของประสิทธิผลในการลด CMV reactivation นอกจากนี้ LTV มี safety profile ที่ดี โดยผู้ป่วยส่วนใหญ่ (ร้อยละ 87.8) ไม่พบอาการไม่พึงประสงค์จากยา adverse effects และมีผลกระทบต่อระดับยาอื่น (drug-drug interactions) อยู่ในระดับจำกัด และสามารถจัดการได้ในทางคลินิก
สำหรับหลักฐานจากการศึกษาในชีวิตจริง (real-world studies) ซึ่งถูกรวบรวมใน systematic review และ meta-analysis ที่ยืนยันผลลัพธ์ดังกล่าวพบว่าการใช้ letermovir สามารถลดทั้งการเกิด CS-CMVi การเกิด cmv reactivation และการเกิด CMV disease7 นอกจากจากผลลัพธ์ด้านการติดเชื้อแล้ว ยังพบประโยชน์ในทางคลินิกอื่น ได้แก่ การลดอัตราการเสียชีวิตจากทุกสาเหตุ การลด non-relapse mortality การลดอุบัติการณ์ GVHD7 แม้ว่าในปัจจุบันยังไม่มีการศึกษาแบบ randomized controlled trial ที่ระบุช่วงเวลาที่เหมาะสมที่สุดในการเริ่มยา letermovir ได้อย่างชัดเจน แต่ข้อมูลจากการศึกษาทางคลินิกหลายฉบับชี้ว่า การเริ่มยาแบบล่าช้า (delayed initiation) มีความสัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นของ CMV reactivation ก่อนเริ่ม prophylaxis8
นอกจากนี้ข้อมูลในผู้ป่วยเด็กมีเพิ่มมากขึ้น โดยเฉพาะในกลุ่มเสี่ยงสูงหลัง HCT หลักฐานจากการศึกษา meta-analysis แสดงให้เห็นว่า letermovir มีทั้งความปลอดภัยและประสิทธิภาพที่ดี โดยพบว่าอุบัติการณ์ของ CS-CMVi ใน 6 เดือนแรกหลัง HCT อยู่ที่ไม่เกินร้อยละ 9.8 และไม่พบการ reactivation ของไวรัสชนิดอื่นเพิ่มขึ้น อย่างไรก็ตามผลต่ออัตราการรอดชีวิต (survival) โดยเฉพาะในกลุ่ม standard risk ยังจำเป็นต้องมีการศึกษาเพิ่มเติม
การตรวจพบ CMV DNAemia ระหว่างการใช้ letermovir
ในผู้ป่วยที่ได้รับ letermovir prophylaxis อาจตรวจพบ CMV DNA ในกระแสเลือดได้ โดยไม่มีหลักฐานของการติดเชื้อจริง (true infection) ภาวะนี้เรียกว่า “letermovir blips”10 กลไกเกิดจากการยับยั้งขั้นตอน viral terminase complex ซึ่งทำหน้าที่ยับยั้งการตัด concatemer DNA ให้เป็น linear genome (terminase inhibition) ส่งผลให้ไวรัสไม่สามารถประกอบเป็นไวรัสตัวใหม่ได้ นำไปสู่การสะสมของ CMV DNA ในรูปแบบ fragmented หรือ non-encapsidated ระดับ CMV DNA ที่พบในลักษณะนี้มักอยู่ในระดับต่ำและสามารถหายได้เอง โดยทั่วไปจะพบระดับไม่เกิน 1,500 IU/mL ใน plasma และไม่เกิน 10,000 IU/mL ใน whole blood11, 12, 13 ภาวะดังกล่าวไม่ถือเป็น breakthrough infection หรือภาวะดื้อยา (drug resistance) ดังนั้น ในกรณีที่ไม่มีหลักฐานทางคลินิกของโรค สามารถพิจารณางดการให้ preemptive therapy ได้
ระยะเวลาการให้ยา letermovir และผลลัพธ์ระยะยาว
การศึกษาแบบ randomized placebo-controlled ในผู้ป่วยเด็กที่ได้รับ letermovir เป็นระยะเวลา 200 วัน พบว่าสามารถลดความเสี่ยงของ CS-CMVi ได้อย่างมีประสิทธิภาพในช่วงที่ได้รับยา อย่างไรก็ตามมีรายงานการเกิด CMV reactivation ภายหลังการหยุดยา (late reactivation) ซึ่งส่งผลให้อุบัติการณ์รวมของ CMV infection ที่ 48 สัปดาห์หลัง HCT ไม่แตกต่างกัน นอกจากนี้อัตราการเสียชีวิตระหว่างกลุ่มที่ได้รับยาและกลุ่มควบคุมไม่แตกต่างกันอย่างมีนัยสำคัญทางสถิติ
ความปลอดภัยและข้อจำกัด15
Letermovir มีจุดเด่นด้านความปลอดภัย โดยพบอาการไม่พึงประสงค์รุนแรงได้ไม่บ่อย และไม่กดการทำงานของไขกระดูก อีกทั้งยังมีปฏิกิริยาระหว่างยากับยาอื่น (drug-drug interactions) ค่อนข้างน้อย อย่างไรก็ตามปัจจุบันยังขาดข้อมูลจากการศึกษาแบบมีกลุ่มควบคุมในผู้ป่วย CMV-seronegative จึงยังไม่แนะนำให้ใช้ letermovir เพื่อการป้องกันในผู้ป่วยกลุ่มนี้ ด้วยประสิทธิภาพที่ดีและความปลอดภัยที่เหนือกว่ายาต้านไวรัสชนิดอื่น letermovir จึงได้รับการพิจารณาเป็น first-line prophylaxis ในผู้ป่วยเด็ก สำหรับกรณีผู้ป่วยที่ไม่เข้าเกณฑ์การให้ CMV prophylaxis ยังคงแนะนำการใช้แนวทางเดิมคือ pre-emptive strategy
ขนาดยาที่แนะนำของ letermovir (dosing recommendations)15
ข้อมูลทางเภสัชจลนศาสตร์ ชี้ให้เห็นว่าอาจจำเป็นต้องมีการปรับขนาดยา letermovir เมื่อมีการเปลี่ยนรูปแบบการให้ยา ระหว่างยารับประทาน (oral) และยาทางหลอดเลือดดำ (intravenous) เพื่อให้ระดับยาในร่างกาย (drug exposure) มีความคงที่และใกล้เคียงกัน อย่างไรก็ตามความจำเป็นในการปรับขนาดยาพบได้เฉพาะในเด็กที่มีอายุน้อยกว่า 12 ปี และมีน้ำหนักตัวน้อยกว่า 30 กิโลกรัม โดยเฉพาะในกรณีที่ไม่ได้รับยา letermovir ร่วมกับ cyclosporine ซึ่งเป็นยากดภูมิคุ้มกันที่มีผลต่อระดับยา ทั้งนี้ข้อมูลดังกล่าวอ้างอิงจากเอกสารกำกับยา (package insert)16 ของ letermovir
ปัจจุบันยา letermovir มี 2 ขนาด คือ oral pellet 20 และ 120 มิลลิกรัม ซึ่งช่วยเพิ่มความสะดวกในการใช้ยา โดยเฉพาะในผู้ป่วยที่ต้องการขนาดยาน้อยกว่า 120 มิลลิกรัม หรือผู้ที่ไม่สามารถกลืนยาเม็ดได้ โดยสามารถให้ยา oral pellet ทางปากร่วมกับอาหารอ่อน (soft food) ก่อนรับประทาน16 ขนาดยาของ letermovir ในผู้ป่วยเด็กแสดงไว้ในตารางที่ 1
ตารางที่ 1 ขนาดยา letermovir ในผู้ป่วยเด็ก15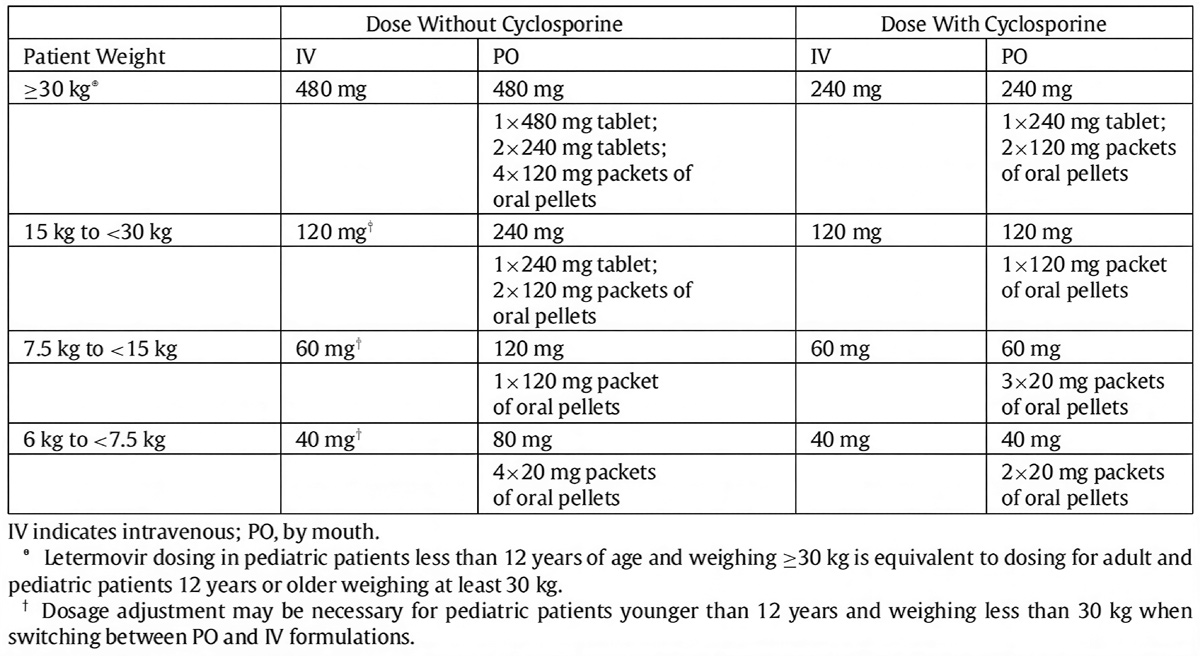
ข้อควรระวังในการใช้ letermovir
การใช้ยา letermovir ในผู้ป่วย HCT ควรพิจารณาอย่างระมัดระวัง โดยเฉพาะประเด็นอันตรกิริยาระหว่างยา (drug–drug interactions) เนื่องจากผู้ป่วยกลุ่มนี้มักได้รับยาหลายชนิดร่วมกัน โดยเฉพาะ ยากดภูมิคุ้มกันและยาต้านเชื้อรา ซึ่งอาจส่งผลต่อระดับยา และความปลอดภัยในการรักษา มีหลักฐานการใช้ letermovir ร่วมกับยากดภูมิคุ้มกัน ได้แก่ cyclosporine, tacrolimus และ sirolimus สามารถเพิ่มค่า area under the curve (AUC) ของยาเหล่านี้ได้ โดยกลไกหลักเกิดจากการยับยั้งเอนไซม์ CYP3A (CYP3A inhibition) ของ letermovir ส่งผลให้การเมแทบอลิซึมของยาลดลงและระดับยาในเลือดสูงขึ้น ซึ่งอาจเพิ่มความเสี่ยงต่อการเกิดพิษจากยา ดังนั้นจึงควรมีการติดตามระดับยาในเลือด (therapeutic drug monitoring; TDM) และพิจารณาปรับขนาดยากดภูมิคุ้มกันอย่างเหมาะสม17 ในทางกลับกัน cyclosporine ยังสามารถเพิ่มระดับ letermovir ในเลือดได้ โดยเกิดจากการยับยั้งตัวขนส่งยา OATP1B1/3 ซึ่งมีบทบาทในการกำจัด letermovir ส่งผลให้ค่า AUC ของยาเพิ่มขึ้น ดังนั้นเมื่อให้ letermovir ร่วมกับ cyclosporine จึงแนะนำให้ลดขนาดยา letermovir ลงเหลือ 240 มิลลิกรัมต่อวัน เพื่อป้องกันระดับยาที่สูงเกินไป17
นอกจากนี้การใช้ letermovir ร่วมกับ voriconazole ต้องใช้ความระมัดระวัง เนื่องจาก letermovir สามารถลดค่า AUC และระดับยา voriconazole ในเลือดได้ โดยมีกลไกจากการกระตุ้นเอนไซม์ CYP2C9 และ CYP2C19 (enzyme induction) ส่งผลให้ voriconazole ถูกเมแทบอลิซึมเร็วขึ้นและระดับยาลดลง ดังนั้น ในกรณีที่จำเป็นต้องใช้ letermovir ร่วมกับ voriconazole ควรมีการติดตามระดับยา voriconazole ในเลือดอย่างใกล้ชิด โดยเฉพาะในช่วง 2 สัปดาห์แรกหลังเริ่มการรักษา หรือหลังเริ่มให้ letermovir เพื่อให้สามารถปรับขนาดยาได้อย่างเหมาะสม16
สรุป
ปัจจุบันแนะนำการใช้ยา letermovir prophylaxis ในผู้ป่วยเด็กที่ได้รับการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือดแบบ allo-HCT เฉพาะในผู้ป่วยที่มีสถานะ CMV seropositive (R+) ซึ่งเป็นแนวทางที่มีประสิทธิภาพและความปลอดภัย อย่างไรก็ตามการเลือกขนาดยา และรูปแบบการให้ยาควรพิจารณาจากข้อมูลทางเภสัชจลนศาสตร์ร่วมกับลักษณะเฉพาะของผู้ป่วยแต่ละราย เพื่อให้ได้ผลลัพธ์การรักษาที่เหมาะสมสูงสุด และลดความเสี่ยงจากอาการไม่พึงประสงค์
- Ljungman P, Alain S, Chemaly R et al. Recommendations from the 10th European Conference on Infections in Leukaemia for the management of cytomegalovirus in patients after allogeneic haematopoietic cell transplantation and other T-cell-engaging therapies, The Lancet Infectious Diseases, 2025; 25, e451-e462.
- Piret, J.; Boivin, G. Management of Cytomegalovirus Infections in the Era of the Novel Antiviral Players, Letermovir and Maribavir. Infect. Dis. Rep. 2024, 16, 65-82.
- Ljungman P, Schmitt M, Marty FM, et al. A mortality analysis of letermovir prophylaxis for cytomegalovirus (CMV) in CMVseropositive recipients of allogeneic hematopoietic cell transplantation. Clin Infect Dis 2020; 70: 1525–33.
- Marty FM, Ljungman P, Chemaly RF, et al. Letermovir prophylaxis for cytomegalovirus in hematopoietic-cell transplantation. N Engl J Med 2017; 377: 2433–44.
- Groll AH, Danziger-Isakov L, Gefen A, Fraser CJ, Schulte JH, Bielorai B, Karras NA, Bueno D, Shaw PJ, Broyde N, Haber B, Gilbert CL, Patel M, McCrea JB, Badshah C. Cytomegalovirus prophylaxis with letermovir in pediatric (birth to <18 years of age) hematopoietic cell transplant recipients: pharmacokinetics, efficacy, and safety results of a Phase 2b study. Antimicrob Agents Chemother. 2025 Oct;69(10):e0042025. doi: 10.1128/aac.00420-25. Epub 2025 Aug 18. PMID: 40824644; PMCID: PMC12486802.
- Chen TT, David AP, Barthelmess EK, MacBrayne CE. Letermovir for cytomegalovirus prophylaxis in pediatric hematopoietic stem cell transplantation. Pediatr Blood Cancer. 2023.
- Vyas A, Raval AD, Kamat S, LaPlante K, Tang Y, Chemaly RF. Real-world outcomes associated with letermovir use for cytomegalovirus primary prophylaxis in allogeneic hematopoietic cell transplant recipients: a systematic review and meta-analysis of observational studies. Open Forum Infect Dis 2022; 10: ofac687.
- Marty FM, Ljungman PT, Chemaly RF, et al. Outcomes of patients with detectable CMV DNA at randomization in the phase III trial of letermovir for the prevention of CMV infection in allogeneic hematopoietic cell transplantation. Am J Transplant 2020; 20: 1703–11.
- Cassaniti I, Colombo AA, Bernasconi P, et al. Positive HCMV DNAemia in stem cell recipients undergoing letermovir prophylaxis is expression of abortive infection. Am J Transplant 2021; 21: 1622–28.
- Yan B, Sun G, Wu Y, et al. Letermovir prophylaxis reduced cytomegalovirus reactivation and resistance post umbilical cord blood transplantation. Br J Haematol 2024; 204: 2378–89.
- Gimenez E, Guerreiro M, Torres I, et al. Features of cytomegalovirus DNAemia and virus-specific T-cell responses in allogeneic hematopoietic stem-cell transplant recipients during prophylaxis with letermovir. Transpl Infect Disease 2023; 25: e14021.
- Studer U, Khanna N, Leuzinger K, et al. Incidence of CMV replication and the role of letermovir primary/secondary prophylaxis in the early phase after allogeneic hematopoietic stem cell transplantation—a single centre study. Anticancer Res 2020; 40: 5909–17.
- Russo D, Schmitt M, Pilorge S, et al. Efficacy and safety of extended duration letermovir prophylaxis in recipients of haematopoietic stem-cell transplantation at risk of cytomegalovirus infection: a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Haematol 2024; 11: e127–35.
- Khawaja F, Zamora D, Yong M et al. American Society for Transplantation and Cellular Therapy Series #11: Updated Cytomegalovirus Guidelines in Hematopoietic Cell Transplant and Cellular Therapy Recipients Transplantation and Cellular Therapy, Official Publication of the American Society for Transplantation and Cellular Therapy, 2025; 31, 727-741.
- Merck Sharp & Dohme Limited. Summary of product characteristics: Prevymis® [Internet]. [cited 2026 Mar 18]. Available from https://www.merck.com/product/usa/pi_circulars/p/prevymis/prevymis_ifu.pdf.
- McCrea JB, Macha S, Adedoyin A, Marshall W, Men¬zel K, Cho CR, et al. Pharmacokinetic drug-drug interactions between letermovir and the immuno¬suppressants cyclosporine, tacrolimus, sirolimus, and mycophenolate mofetil. J Clin Pharmacol. 2019;59(10):1331-9.