รศ. พญ. ชุตินธร ศรีพระประแดง
รศ. พญ. ชุตินธร ศรีพระประแดง
สาขาวิชาโรคต่อมไร้ท่อและเมแทบอลิซึม ภาควิชาอายุรศาสตร์
คณะแพทยศาสตร์โรงพยาบาลรามาธิบดี
ในเดือนสิงหาคม 2568 ที่ผ่านมา American Thyroid Association (ATA) ได้ตีพิมพ์ guidelines เรื่อง differentiated thyroid cancer ที่ปรับปรุงจากฉบับเดิมเมื่อ 10 ปีก่อน โดยมีรายละเอียดมากกว่าเดิม ครอบคลุมเนื้อหากว่า 150 หน้า บทความนี้ขอสรุปประเด็นสำคัญที่แพทย์ผู้ดูแลผู้ป่วยมะเร็งต่อมไทรอยด์ควรทราบค่ะ
2025 ATA Management Guidelines for Adult Patients with Differentiated Thyroid Cancer
Guideline นี้เป็นการอัปเดตจาก ATA guideline ปี ค.ศ. 2015 โดยแยกส่วนของ thyroid nodule ออกไป (ซึ่ง guideline ของ thyroid nodule ฉบับใหม่ยังไม่เผยแพร่ในขณะนี้) ทั้งนี้ guideline ฉบับปัจจุบันนี้อ้างอิงหลักฐานเชิงประจักษ์ (evidence-based) และจัดทำโดยมีการทบทวนวรรณกรรมอย่างเป็นระบบ เพื่อเป็นแนวทางการจัดการผู้ป่วยมะเร็งต่อมไทรอยด์ชนิด differentiated (DTC) ในผู้ใหญ่ ซึ่งครอบคลุมทั้ง papillary, follicular และ oncocytic carcinoma ภายใต้กรอบแนวคิด “DATA” framework ได้แก่ Diagnosis – Assessment of risk/benefit for treatment vs. active surveillance or monitoring – Treatment – Assessment to response
1. การประเมินความเสี่ยง (Risk stratification and assessment)
การประเมินเริ่มต้นใช้ระบบ 2025 ATA Risk Stratification System เพื่อประเมินความเสี่ยงของ structural disease persistence หรือ recurrence แบ่งเป็น 4 ระดับ ได้แก่ Low (<10%); Low-intermediate (10 – 15%); Intermediate-high (16 – 30%); High (>30%) โดยระบบใหม่นี้ใช้ข้อมูลการศึกษาล่าสุดเพื่อคาดการณ์ความเสี่ยงของ recurrence ได้ดีขึ้น
สำหรับการประเมินความเสี่ยงในระยะยาว ใช้ dynamic risk assessment เพื่อติดตามการตอบสนองต่อการรักษา หากมี excellent response สามารถปรับเป้าหมายของ TSH ให้อยู่ในเกณฑ์ปกติและในกลุ่ม ATA low risk สามารถพิจารณาติดตาม imaging ห่างขึ้นได้
NIFTP (Noninvasive Follicular Thyroid Neoplasm with Papillary-like Nuclear Features) จัดเป็น neoplasm ที่มี very low malignant potential
2. การรักษาเริ่มต้น (Initial Treatment)
หลักการรักษาที่สำคัญ คือ การลดความเสี่ยงการกลับเป็นซ้ำ โดยลดผลข้างเคียงของการรักษาให้น้อยที่สุด และให้ผู้ป่วยมีส่วนร่วมในการตัดสินใจ (shared decision-making)
- cT1N0M0 (≤2 cm): แนะนำ thyroid lobectomy เนื่องจากภาวะแทรกซ้อนน้อยกว่า total thyroidectomy แต่หากมีรอยโรคทั้งสองข้างหรือมี multifocality แนะนำ total thyroidectomy
- cT2N0M0 (>2–4 cm): เลือกได้ทั้ง lobectomy หรือ total thyroidectomy โดยข้อดีของ total thyroidectomy คือ สามารถให้ radioactive iodine หรือติดตามระดับ thyroglobulin ได้ง่าย
- Advanced disease (cT3-4, cN1, cM1): แนะนำ total thyroidectomy neck dissection
Active surveillance เหมาะกับผู้ป่วย papillary thyroid carcinoma ขนาด ≤1 cm ที่มีความเสี่ยงต่ำ
Percutaneous Ablation (เช่น radiofrequency ablation หรือ RFA) เป็นทางเลือกแทน active surveillance หรือการผ่าตัดในรายที่เหมาะสม
- Prophylactic central lymph node dissection ไม่แนะนำให้ทำเป็น routine procedure ใน papillary thyroid carcinoma หรือ follicular thyroid carcinoma ที่มีขนาดเล็ก ไม่ invasive และ ไม่พบต่อมน้ำเหลืองโต (cT1-2, cN0)
- Therapeutic lymph node dissection แนะนำเฉพาะในรายที่ตรวจพบต่อมน้ำเหลืองโตบริเวณ central หรือ lateral neck nodes
3. Adjuvant therapy ด้วย radioactive iodine
- Low-risk: ไม่แนะนำให้ radioactive iodine เป็น routine therapy หลังการผ่าตัด total thyroidectomy
- Intermediate-risk: พิจารณาเป็นราย ๆ โดยจะให้ radioactive iodine ในรายที่มี aggressive histology หรือมี extensive nodal disease
- High-risk/distant metastases: แนะนำให้ radioactive iodine เป็น routine therapy หลังการผ่าตัด total thyroidectomy
การเตรียมตัวก่อน radioactive iodine: ควรรับประทานอาหารที่มีไอโอดีนต่ำ 1–2 สัปดาห์ และกระตุ้นให้ TSH >30 mIU/L โดยการหยุดฮอร์โมนไทรอยด์หรือใช้ recombinant human (rhTSH)
4. การดูแลรักษาและติดตามระยะยาว
TSH Suppression Therapy
ควรปรับระดับ TSH suppression ตามความเสี่ยงของผู้ป่วย โดยหลีกเลี่ยงการเกิด subclinical hyperthyroidism ซึ่งเพิ่มความเสี่ยงต่อ atrial fibrillation หรือ osteoporosis โดยไม่จำเป็น ผู้ป่วยที่มี lowหรือ intermediate risk และมี excellent response ไม่จำเป็นต้องให้ TSH suppression therapy โดยสามารถปรับให้ระดับ TSH อยู่ในเกณฑ์ปกติก็เพียงพอ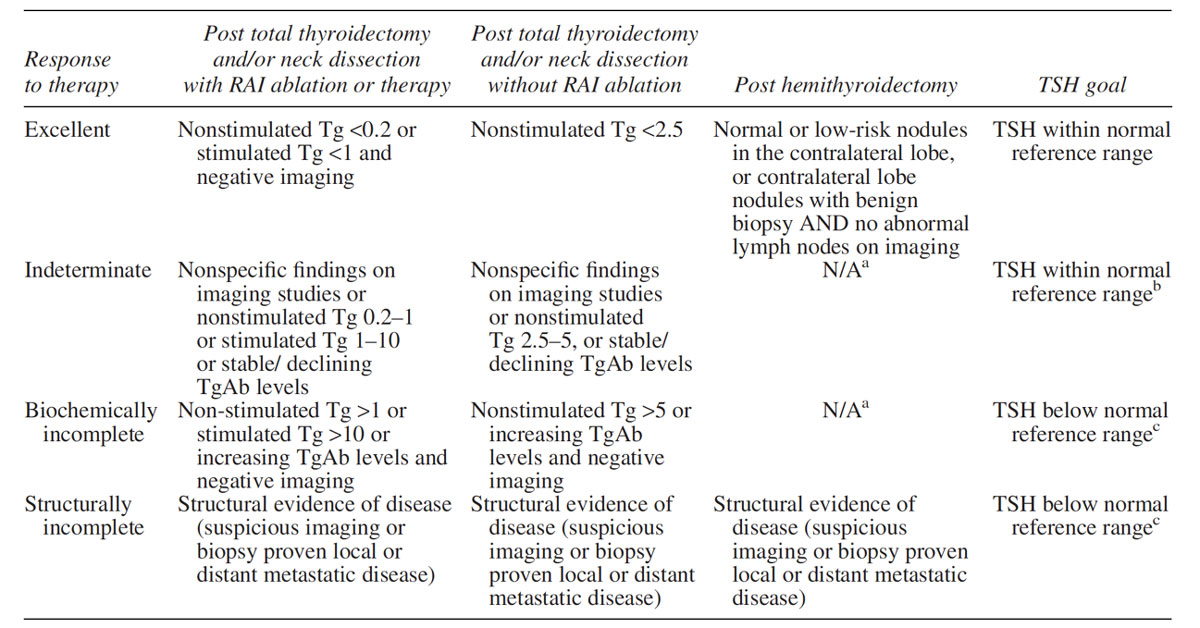
- ติดตามครั้งแรกภายใน 3 เดือนหลังผ่าตัด เพื่อพิจารณาความจำเป็นในการให้ radioactive iodine และการดูแลรักษาอื่น ๆ เพิ่มเติม
- Imaging: ทำ neck ultrasound หลังการรักษาประมาณ 6 – 12 เดือน
- Tumor marker: ตรวจ serum thyroglobulin หลัง total thyroidectomy ประมาณ 6 – 12 สัปดาห์ ไม่ควรตรวจติดตามระดับ thyroglobulin หลังผ่าตัด lobectomy
- ตรวจ thyroglobulin antibody ทุกครั้งที่ตรวจ thyroglobulin เพราะหากเป็นบวก ค่า thyroglobulin อาจต่ำกว่าความเป็นจริง (falsely low) และควรติดตามด้วยการดูแนวโน้มของ antibody แทน
- De-escalation: ผู้ป่วยที่มี excellent response ต่อเนื่อง 10 – 15 ปีหลังผ่าตัด total thyroidectomy อาจพิจารณาว่าโรคสงบและไม่จำเป็นต้องติดตามแบบ routine monitoring ได้
5. Advance disease หรือ radioactive iodine-refractory differentiated thyroid cancer
Therapeutic approach
ควรตรวจ genetic alterations เช่น BRAFV600E mutation, RET, NTRK fusion เพื่อพิจารณาการให้ systemic therapy หากไม่พบ genetic alterations ที่สามารถ target ได้ แนะนำใช้ multikinase inhibitors ได้แก่ lenvatinib หรือ sorafenib โดย lenvatinib ถือเป็น first-line therapy ที่ช่วยเพิ่ม progression-free survival ได้ แต่ต้องระวังและจัดการผลข้างเคียงเพื่อลดการหยุดหรือปรับลดขนาดยาโดยไม่จำเป็น
Locoregional Recurrence
ในกรณีที่พบเพียง cervical lymph node metastasis อาจพิจารณาการรักษาเฉพาะที่ เช่น ผ่าตัด, radiofrequency ablation (RFA) หรือ percutaneous ethanol injection (PEI) แทนการให้ radioactive iodine ซ้ำ ๆ
6. การดูแลด้านคุณภาพชีวิต
ผู้ป่วยมะเร็งต่อมไทรอยด์จำนวนมากมีปัญหาทางจิตใจและคุณภาพชีวิตลดลง เช่น ความวิตกกังวล ความเครียดและภาระค่าใช้จ่าย แพทย์ควรประเมินและให้การช่วยเหลือด้านจิตใจควบคู่กับการรักษาทางกาย เพื่อให้ผู้ป่วยมีคุณภาพชีวิตที่ดีในระยะยาว
เอกสารอ้างอิง
Ringel MD, Sosa JA, Baloch Z, et al. 2025 American Thyroid Association Management Guidelines for Adult Patients with Differentiated Thyroid Cancer. Thyroid. 2025;35(8):841-985.