 พญ. ทักษพร แสงจัน
พญ. ทักษพร แสงจัน
หน่วยโรคติดเชื้อ ภาควิชากุมารเวชศาสตร์
คณะแพทยศาสตร์ศิริราชพยาบาลพยาบาล
 รศ. พญ. วนัทปรียา พงษ์สามารถ
รศ. พญ. วนัทปรียา พงษ์สามารถ
หน่วยโรคติดเชื้อ ภาควิชากุมารเวชศาสตร์
คณะแพทยศาสตร์ศิริราชพยาบาลพยาบาล
ในช่วงปี พ.ศ. 2568 ที่ผ่านมาประเทศไทยเผชิญกับการระบาดของโรคติดเชื้อทางเดินหายใจหลายชนิด ทั้งไข้หวัดใหญ่ไวรัสอาร์เอสวี (RSV) และสำหรับโควิด 19 แม้จะพบผู้ป่วยน้อยลงมาก แต่ยังคงมีผู้ป่วยเสียชีวิตจากโควิด 19 อยู่ ซึ่งโรคติดเชื้อทางเดินหายใจดังกล่าวมีรูปแบบการระบาดที่เปลี่ยนแปลงไปตามฤดูกาลและระดับการแพร่ระบาดในชุมชน โดยเฉพาะในช่วงปลายปี พ.ศ. 2568 พบการระบาดของโรคไข้หวัดใหญ่อย่างกว้างขวาง ส่งผลให้มียอดผู้ป่วยสะสมทั้งปีสูงถึง 1,194,342 ราย และมีผู้เสียชีวิต 129 ราย1,2 สถานการณ์ดังกล่าวส่งผลกระทบต่อสุขภาพของประชาชนและภาระของระบบสาธารณสุขของประเทศ ผลกระทบดังกล่าวมีความรุนแรงมากยิ่งขึ้นในกลุ่มผู้ป่วยที่มีภาวะภูมิคุ้มกันบกพร่อง เนื่องจากความบกพร่องของกลไกการป้องกันของร่างกายทำให้กลุ่มผู้ป่วยเหล่านี้มีความเสี่ยงต่อการติดเชื้อที่รุนแรง การเข้ารับการรักษาในโรงพยาบาล และการเสียชีวิตสูงกว่าประชากรทั่วไป 3 แม้ว่าวัคซีนจะเป็นมาตรการที่สำคัญในการป้องกันการติดเชื้อและลดความรุนแรงของโรคจากการติดเชื้อโควิด 19 ไข้หวัดใหญ่ และไวรัสอาร์เอสวี แต่ประสิทธิผลของวัคซีนในผู้ป่วยภูมิคุ้มกันบกพร่องมักต่ำกว่าผู้ที่มีภูมิคุ้มกันปกติ อีกทั้งยังมีข้อจำกัดด้านความรู้ความเข้าใจเกี่ยวกับความปลอดภัย ประสิทธิภาพ และข้อห้ามของการให้วัคซีนในกลุ่มผู้ป่วยภูมิคุ้มกันบกพร่อง ในปี พ.ศ. 2568 ทางสมาคมโรคติดเชื้อแห่งอเมริกา (Infectious Disease Society of America, IDSA) ทบทวนหลักฐานทางวิชาการและจัดทำแนวทางการให้วัคซีนป้องกันโรคโควิด-19 ไข้หวัดใหญ่ และการติดเชื้อ RSV ในผู้ป่วยที่มีภาวะภูมิคุ้มกันบกพร่อง ซึ่งได้แก่ ผู้ป่วยโรคมะเร็งทางโลหิตวิทยา (hematologic malignancy) โรคมะเร็งชนิดก้อน (solid tumor) ผู้ได้รับการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือด (hematopoietic cell transplantation, HCT) ผู้ได้รับการปลูกถ่ายอวัยวะ (solid organ transplant, SOT) ผู้ได้รับการรักษาด้วย chimeric antigen receptor T-cell therapy (CAR-T) ผู้ป่วยโรคภูมิต้านตนเองที่ได้รับยากดภูมิคุ้มกัน ผู้ป่วยภูมิคุ้มกันบกพร่องแต่กำเนิด และผู้ติดเชื้อเอชไอวีที่มีภาวะภูมิคุ้มกันบกพร่องรุนแรง (CD4 <15% หรือ <200 เซลล์/มม.³) ทั้งนี้ ผู้ป่วยโรคเรื้อรัง เช่น โรคไตระยะสุดท้าย โรคตับแข็ง โรคหัวใจ ไม่ถือว่าอยู่ในขอบเขตของแนวทางนี้4 โดยบทความจะกล่าวถึงประสิทธิผลของวัคซีน (vaccine effectiveness, VE) ความปลอดภัย และคำแนะนำการให้วัคซีน ดังนี้
1. วัคซีนป้องกันโรคโควิด 19
การศึกษาประสิทธิผลของวัคซีนทั้งแบบ cohort study และ test-negative case-control study ในผู้ใหญ่ที่มีภาวะภูมิคุ้มกันบกพร่องพบว่าการฉีดวัคซีนป้องกันโรคโควิด 19 ในกลุ่มผู้ที่มีภาวะภูมิคุ้มกันบกพร่อง ลดอัตราการนอนโรงพยาบาลจากการติดเชื้อโควิด 19 ร้อยละ 33 – 565-8 ลดการเจ็บป่วยรุนแรงร้อยละ 40 และการลดอัตราการเสียชีวิตร้อยละ 618 ดังนั้น ผู้ใหญ่และเด็กที่มีภาวะภูมิคุ้มกันบกพร่อง แนะนำฉีดวัคซีนป้องกันโรคโควิด 19 สำหรับฤดูกาลปี ค.ศ. 2025 – 2026 ตามความเหมาะสมของช่วงอายุ (strong recommendation, moderate certainty of evidence)
ด้านความปลอดภัยและอาการไม่พึงประสงค์ วัคซีนป้องกันโรคโควิด 19 ที่มีใช้อยู่ในปัจจุบัน ไม่พบความสัมพันธ์กับการเกิดอาการไม่พึงประสงค์ร้ายแรง ความเสี่ยงของอาการไม่พึงประสงค์บางอย่างที่รายงานเพิ่มขึ้นหลังได้รับวัคซีนเข็มที่สามเมื่อวิเคราะห์ทางสถิติพบว่าไม่มีความสัมพันธ์อย่างแท้จริงกับวัคซีน เนื่องจากมีการประเมินหลายภาวะและอัตราการเกิดเหตุการณ์ต่ำ9 ส่วนเหตุการณ์ไม่พึงประสงค์สำคัญ เช่น ภาวะลิ่มเลือดอุดตัน กล้ามเนื้อหัวใจตาย และโรคหลอดเลือดสมอง พบในกลุ่มผู้ได้รับวัคซีนน้อยกว่ากลุ่มที่ไม่ได้รับวัควีน ซึ่งสะท้อนถึงความเสี่ยงที่เพิ่มขึ้นจากการติดเชื้อโควิด 19 เอง นอกจากนี้ โดยทั่วไปไม่พบว่าวัคซีนทำให้เกิดการกำเริบของโรคในผู้ที่มีภาวะภูมิคุ้มกันบกพร่องหรือโรคภูมิต้านตนเอง โดยภาพรวมจึงสรุปได้ว่าวัคซีนป้องกันโรคโควิด 19 มีความปลอดภัย และมีความเสี่ยงของเหตุการณ์ไม่พึงประสงค์ร้ายแรงอยู่ในระดับต่ำมาก10,11
- แนะนำฉีดวัคซีนป้องกันโรคโควิด 19 สายพันธุ์ล่าสุด โดยพิจารณาตามประวัติการได้รับวัคซีนและชนิดของวัคซีน นอกจากนี้การให้วัคซีนโดสที่สองอาจช่วยเพิ่มระยะเวลาการป้องกันโรคได้
- ควรฉีดวัคซีนป้องกันโรคโควิด 19 สายพันธุ์ล่าสุด ให้แก่สมาชิกในบ้านและผู้ใกล้ชิดกับผู้ป่วยที่มีภูมิคุ้มกันบกพร่อง
- มาตรการเสริมที่มีความสำคัญ โดยเฉพาะผู้ที่มีการตอบสนองต่อวัคซีนไม่ดีหรือมีข้อห้ามในการรับวัคซีน ได้แก่
การเข้าถึงยาต้านไวรัส และมาตรการป้องกันโรคที่ไม่ใช้ยา (non-pharmaceutical interventions) เช่น การสวมหน้ากากอนามัย และการล้างมือ เป็นต้น
2. วัคซีนป้องกันไข้หวัดใหญ่
การศึกษาประสิทธิผลของวัคซีนแบบ case-control study ในผู้ใหญ่ที่มีภาวะภูมิคุ้มกันบกพร่อง พบว่าการฉีดวัคซีนป้องกันโรคไข้หวัดใหญ่ ลดการนอนโรงพยาบาลจากไข้หวัดใหญ่ร้อยละ 3212 ลดการเข้ารักษาในหอผู้ป่วยวิกฤต (ICU) ร้อยละ 4112,13 ลดอัตราการเสียชีวิตจากทุกสาเหตุในผู้สูงอายุร้อยละ 5312 ดังนั้น ผู้ใหญ่และเด็กที่มีภาวะภูมิคุ้มกันบกพร่อง แนะนำฉีดวัคซีนป้องกันไข้หวัดใหญ่ประจำฤดูกาลให้เหมาะสมตามช่วงอายุ และควรได้รับการฉีดกระตุ้นทุกปีเพื่อให้ได้รับการป้องกันที่มีประสิทธิภาพที่สุด (strong recommendation, moderate certainty of evidence)
ด้านความปลอดภัยและอาการไม่พึงประสงค์ วัคซีนไข้หวัดใหญ่ไม่มีหลักฐานของการเพิ่มความเสี่ยงของกลุ่มอาการ Guillain-Barre syndrome14 และโรคหลอดเลือดสมองอย่างมีนัยสำคัญ และยังมีหลักฐานจากการศึกษาแบบ cohort study พบว่าการได้รับวัคซีนไข้หวัดใหญ่ภายใน 30 วันมีความสัมพันธ์กับการลดลงของความเสี่ยงต่อโรคหลอดเลือดสมอง15 นอกจากนี้ วัคซีนยังมีความปลอดภัยในผู้ที่มีภาวะภูมิคุ้มกันบกพร่องหรือโรคภูมิต้านตนเอง โดยไม่พบการกำเริบของโรคหรือผลกระทบทางคลินิกที่สำคัญ เช่น ในผู้ป่วยปลูกถ่ายไตไม่พบการเปลี่ยนแปลงของการทำงานของไต (eGFR, serum creatinine หรือ proteinuria) และไม่พบภาวะเม็ดเลือดขาวต่ำ นิวโทรฟิลต่ำ หรือเกล็ดเลือดต่ำหลังการได้รับวัคซีน เป็นต้น16
- พิจารณาฉีดวัคซีนป้องกันไข้หวัดใหญ่ชนิดขนาดสูง (high-dose) ตามความเหมาะสมของอายุ เนื่องจากช่วยกระตุ้นการตอบสนองของระบบภูมิคุ้มกันได้เพิ่มขึ้น ซึ่งมีความสำคัญในผู้ป่วยที่มีภาวะภูมิคุ้มกันบกพร่อง
- ห้ามใช้วัคซีนป้องกันไข้หวัดใหญ่ชนิดเชื้อเป็นอ่อนฤทธิ์ (live-attenuated influenza vaccine)ในผู้ที่มีภาวะภูมิคุ้มกันบกพร่อง และควรหลีกเลี่ยงในผู้ใกล้ชิดกับผู้ที่มีภาวะภูมิคุ้มกันบกพร่องรุนแรง เช่น ผู้ป่วยที่เพิ่งได้รับการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือด (HCT) ผู้ป่วยที่มีภาวะ GVHD (graft versus host disease) ผู้ป่วยที่มีภาวะภูมิคุ้มกันบกพร่องรวมชนิดรุนแรง (severe combined immunodeficiency, SCID) เป็นต้น
- ควรฉีดวัคซีนป้องกันไข้หวัดใหญ่ให้แก่สมาชิกในบ้านและผู้ใกล้ชิดกับผู้ป่วยที่มีภูมิคุ้มกันบกพร่อง
- มาตรการเสริมที่มีความสำคัญ โดยเฉพาะผู้ที่มีการตอบสนองต่อวัคซีนไม่ดีหรือมีข้อห้ามในการรับวัคซีน ได้แก่
การเข้าถึงยาต้านไวรัส และมาตรการป้องกันโรคที่ไม่ใช้ยา (non-pharmaceutical interventions)
3. วัคซีนป้องกัน RSV
การศึกษาประสิทธิผลของวัคซีนแบบ case-control study ในผู้ใหญ่ที่มีภาวะภูมิคุ้มกันบกพร่องพบว่าวัคซีนป้องกัน RSV ลดการนอนโรงพยาบาลจากการติดเชื้อ RSV ถึงร้อยละ 7017,18 ดังนั้น ในผู้ใหญ่และวัยรุ่นที่มีภาวะภูมิคุ้มกันบกพร่อง แนะนำให้วัคซีนป้องกัน RSV ตามความเหมาะสมของช่วงอายุ (strong recommendation, moderate certainty of evidence)
แม้ว่าจะมีการศึกษาแบบ self-controlled case series หนึ่งการศึกษารายงานความเสี่ยงของกลุ่มอาการ Guillain-Barré syndrome เพิ่มขึ้นหลังการได้รับวัคซีน แต่ความเสี่ยงเชิงปริมาณอยู่ในระดับต่ำมาก คือ 11.2 รายต่อการให้วัคซีน 1,000,000 โดส18 นอกจากนี้หลักฐานจากการศึกษาแบบ randomized controlled trials หลายการศึกษาชี้ให้เห็นว่าวัคซีนไม่เพิ่มความเสี่ยงของเหตุการณ์ไม่พึงประสงค์ร้ายแรง เมื่อเทียบกับผู้ที่ไม่ได้รับวัคซีน
- วัคซีนป้องกันRSV สำหรับผู้ใหญ่ที่ได้รับการรับรองจากองค์การอาหารและยาในสหรัฐอเมริกา ได้แก่ RSVPreF3, RSVPreF และ mRNA-1345 แนะนำให้ฉีดเพียง 1 เข็ม โดยแนะนำให้ฉีดก่อนเข้าฤดูกาลระบาด สำหรับประเทศไทยมักระบาดในช่วงเดือนกรกฎาคมถึงพฤศจิกายน ทั้งนี้ฤดูกาลระบาดอาจมีการเปลี่ยนแปลงตามภูมิภาคและสภาวะอากาศโลก19
- ผู้ป่วยที่มีภาวะภูมิคุ้มกันบกพร่องทุกคนที่มีอายุตั้งแต่ 18 ปีขึ้นไป ควรได้รับวัคซีนป้องกัน RSV
- ผู้ป่วยที่มีภาวะภูมิคุ้มกันบกพร่องอายุน้อยกว่า 18 ปี ควรพิจารณาการฉีดโดยอาศัยการตัดสินใจร่วมกันระหว่างแพทย์และผู้ป่วย/ผู้ปกครอง
- ผู้ที่รอการปลูกถ่ายอวัยวะ โดยเฉพาะการปลูกถ่ายปอด ควรได้รับวัคซีนป้องกัน RSV ก่อนการปลูกถ่าย
- ควรฉีดวัคซีนป้องกัน RSV ให้แก่สมาชิกในครัวเรือนและผู้ใกล้ชิดกับผู้ป่วยที่มีภูมิคุ้มกันบกพร่อง หากมีข้อบ่งชี้สำหรับตนเอง
- มาตรการเสริมที่มีความสำคัญ โดยเฉพาะผู้ที่มีการตอบสนองต่อวัคซีนไม่ดีหรือมีข้อห้ามในการรับวัคซีน ได้แก่ การเข้าถึงการรักษาด้วยอิมมูโนโกลบูลิน (immunoglobulin) อย่างรวดเร็ว และการใช้มาตรการที่ป้องกันโรคไม่ใช้ยา (non-pharmaceutical interventions)
ตารางที่ 1 แนวทางการฉีดวัคซีนป้องกันโรคโควิด 19 ไข้หวัดใหญ่ และการติดเชื้อ RSV ในผู้ป่วยที่มีภาวะภูมิคุ้มกันบกพร่อง โดยแบ่งตามกลุ่มโรคและการรักษาที่ได้รับ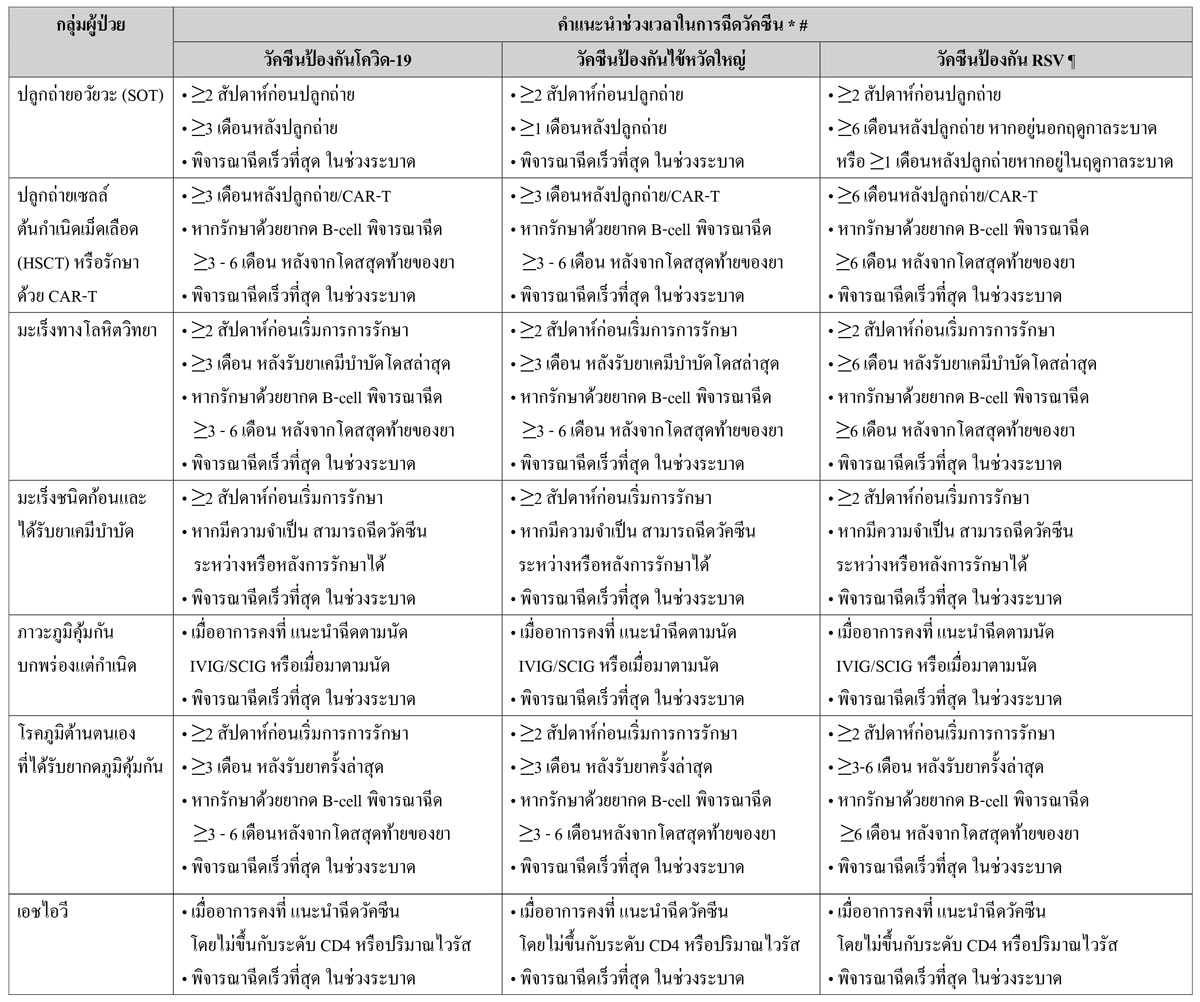
* หลีกเลี่ยงช่วงที่ได้รับยากดภูมิขนาดสูง ช่วงรักษาภาวะปฏิเสธอวัยวะปลูกถ่ายเฉียบพลัน (acute transplant rejection)
ช่วงโรคภูมิต้านตนเองกำเริบรุนแรง หรือมีอาการเจ็บป่วยรุนแรงหรือเฉียบพลัน
# ผู้ป่วยสามารถรับวัคซีนป้องกันโควิด-19 วัคซีนป้องกันไข้หวัดใหญ่ และวัคซีนป้องกัน RSV พร้อมกันได้อย่างเหมาะสม
¶ หากฉีดวัคซีนป้องกัน RSV เร็วกว่าช่วงที่เหมาะสม อาจพิจารณา ให้วัคซีนซ้ำ (re-dose) ยกเว้น กลุ่มภูมิคุ้มกันบกพร่องแต่กำเนิด
โดยสรุป
แนวทางนี้จะช่วยให้บุคลากรทางการแพทย์สามารถประเมินประโยชน์และความเสี่ยงของการให้วัคซีนป้องกันโควิด-19 ไข้หวัดใหญ่ และ RSV ในผู้ป่วยที่มีภาวะภูมิคุ้มกันบกพร่องได้อย่างเหมาะสม โดยคำนึงถึงระดับความบกพร่องของภูมิคุ้มกัน ชนิดของโรคประจำตัว วิธีการรักษาที่ได้รับ และช่วงเวลาที่เหมาะสมในการให้วัคซีน แนวทางนี้ยังสนับสนุนการตัดสินใจร่วมกันระหว่างแพทย์ ผู้ป่วย และครอบครัว เพื่อให้เกิดความเข้าใจที่ถูกต้องเกี่ยวกับประสิทธิผลและความปลอดภัยของวัคซีน อันจะนำไปสู่การป้องกันโรคติดเชื้อทางเดินหายใจได้อย่างมีประสิทธิภาพ ลดความรุนแรงของโรค ลดอัตราการนอนโรงพยาบาล และเพิ่มความปลอดภัยของผู้ป่วยในกลุ่มเสี่ยงเหล่าบางนี้ในระยะยาว
- กองระบาดวิทยา กรมควบคุมโรค. รายงานผลการเฝ้าระวังไข้หวัดใหญ่และเชื้อสาเหตุโรคติดเชื้อทางเดินหายใจ ปี 2568 [อินเตอร์เน็ต]. 2568. [สืบค้นเมื่อวันที่ 14 ม.ค. 2568]. จาก: https://ddc.moph.go.th/uploads/ckeditor2//files/DOE_fluproject_biweekly_wk51-52.pdf
- กองระบาดวิทยา กรมควบคุมโรค. รายงานสถานการณ์โรคไข้หวัดใหญ่ ประเทศไทย พ.ศ. 2568 [อินเตอร์เน็ต]. 2568. [สืบค้นเมื่อวันที่ 14 ม.ค. 2568]. จาก: https://ddc.moph.go.th/uploads/ckeditor2//files/DOE_flu_53.2568.pdf
- Azoulay E, Russell L, Van de Louw A, Metaxa V, Bauer P, Povoa P, et al. Diagnosis of severe respiratory infections in immunocompromised patients. Intensive Care Med. 2020 Feb;46(2):298-314
- Infectious Diseases Society of America. IDSA 2025 Guidelines on the Use of Vaccines for the Prevention of Seasonal COVID-19, Influenza, and RSV Infections in Immunocompromised Patients [Internet]. 2025 November. [cited 2026 Jan 9]. Available from: https://www.idsociety.org/Seasonal-RTI-Vaccinations-in-Immunocompromised-Patients/
- Wilson A, Rahai N, Beck E, Beebe E, Conroy B, Esposito D, et al. Evaluating the Effectiveness of mRNA-1273.815 Against COVID-19 Hospitalization Among Adults Aged ≥ 18 Years in the United States. Infect Dis Ther. 2025 Jan;14(1):199-216.
- Link-Gelles R, Rowley EA, DeSilva MB, et al. Interim Effectiveness of Updated 2023–2024 (Monovalent XBB.1.5) COVID-19 Vaccines Against COVID-19–Associated Hospitalization Among Adults Aged ≥18 Years with Immunocompromising Conditions, VISION Network, September 2023–February 2024. MMWR Morb Mortal Wkly Rep 2024;73:271–276.
- Nguyen JL, Mitratza M, Volkman HR, de Munter L, Tran TMP, Marques C, et al. Effectiveness of the BNT162b2 XBB.1.5-adapted vaccine against COVID-19 hospitalization related to the JN.1 variant in Europe: a test-negative case-control study using the id.DRIVE platform. EClinicalMedicine. 2024 Dec 9;79:102995.
- Link-Gelles R, Rowley EAK, Irving SA, Klein NP, Grannis SJ, Ong TC, et al. Estimated 2023-2024 COVID-19 Vaccine Effectiveness in Adults. JAMA Netw Open. 2025 Jun 2;8(6):e2517402.
- Chen DT, Copland E, Hirst JA, Mi E, Dixon S, Coupland C, Hippisley-Cox J. Uptake, effectiveness and safety of COVID-19 vaccines in individuals at clinical risk due to immunosuppressive drug therapy or transplantation procedures: a population-based cohort study in England. BMC Med. 2024 Jun 10;22(1):237.
- Rossier LN, Décosterd NP, Matter CB, Staudenmann DA, Moser A, Egger B, Seibold FW. SARS-CoV-2 vaccination in inflammatory bowel disease patients is not associated with flares: a retrospective single-centre Swiss study. Ann Med. 2024 Dec;56(1):2295979.
- Ganelin-Cohen E, Buxbaum C, Bosak N, Sobol S, Vaknin-Dembinsky A, Hellmann MA, et al. The effect of COVID-19 vaccination on multiple sclerosis activity as reflected by MRI. Brain Behav. 2024 Jul;14(7):e3587.
- Lewis NM, Harker EJ, Cleary S, Zhu Y, Grijalva CG, Chappell JD, et al. Vaccine Effectiveness Against Influenza A(H1N1), A(H3N2), and B-Associated Hospitalizations, United States, 1 September 2023 to 31 May 2024. J Infect Dis. 2025 Oct 15;232(4):e626-e636.
- Tenforde MW, Reeves EL, Weber ZA, Tartof SY, Klein NP, Dascomb K, et al. Influenza Vaccine Effectiveness Against Hospitalizations and Emergency Department or Urgent Care Encounters for Children, Adolescents, and Adults During the 2023-2024 Season, United States. Clin Infect Dis. 2025 Oct 6;81(3):667-678.
- Lloyd PC, Acharya G, Zhao H, Shah N, Anguzu G, Ambarsoomzadeh D, et al. Safety monitoring of health outcomes following influenza vaccination during the 2023-2024 season among U.S. Medicare beneficiaries aged 65 years and older. Vaccine. 2025 Apr 19;53:127069.
- Tanaka K, Demchuk AM, Malo S, Hill MD, Holodinsky JK. Risk of stroke within 3, 7, 14, 21 and 30 days after influenza vaccination in Alberta, Canada: A population-based study. Eur J Neurol. 2024 Apr;31(4):e16172.
- Zawiasa-Bryszewska A, Nowicka M, Górska M, Edyko P, Edyko K, Tworek D, et al. Safety and Efficacy of Influenza Vaccination in Kidney Graft Recipients in Late Period After Kidney Transplantation. Vaccines (Basel). 2025 Feb 14;13(2):189.
- Payne AB, Watts JA, Mitchell PK, Dascomb K, Irving SA, Klein NP, et al. Respiratory syncytial virus (RSV) vaccine effectiveness against RSV-associated hospitalisations and emergency department encounters among adults aged 60 years and older in the USA, October, 2023, to March, 2024: a test-negative design analysis. Lancet. 2024 Oct 19;404(10462):1547-1559.
- Fry SE, Terebuh P, Kaelber DC, Xu R, Davis PB. Effectiveness and Safety of Respiratory Syncytial Virus Vaccine for US Adults Aged 60 Years or Older. JAMA Netw Open. 2025 May 1;8(5):e258322.
- Infectious Disease Association of Thailand. Recommended Adult and Elderly Immunization Schedule. [Internet] 2025 Mar. [cited 2026 Jan 14]. Available from: https://idthai.org/2015/files_upload/files/Recommended%20 Adult%20and%20Elderly%20Immunization%20Schedule%202025%20Web.pdf




