 พ.ท. รศ. นพ. บัญชา สถิระพจน์
พ.ท. รศ. นพ. บัญชา สถิระพจน์
แผนกโรคไต กองอายุรกรรม โรงพยาบาลพระมงกุฎเกล้า
.
สรุปเนื้อหางานประชุม Nephrology Review for Internists 2020 จัดโดย สมาคมโรคไตแห่งประเทศไทย วันที่ 26 กันยายน 2563
บทนำ
ความดันโลหิตสูงเป็นปัญหาที่พบบ่อยในเวชปฏิบัติ จากการศึกษาในประชากรไทย พบว่า ไม่ได้รับการวินิจฉัยความดันโลหิตสูงพบสูงถึงร้อยละ 44.7 และสามารถควบคุมระดับความดันโลหิตได้ต่ำกว่า 140/90 มิลลิเมตรปรอท เพียงประมาณร้อยละ 30 โดยความดันโลหิตสูงเป็นสาเหตุอันดับสองของการเกิดโรคไตเรื้อรังระยะสุดท้ายของประชากรไทย คือ พบประมาณร้อยละ 30 เมื่อระดับความดันโลหิตตัวบนมากกว่า 150 มิลลิเมตรปรอทจะเพิ่มความเสี่ยงต่อการเกิดโรคไตเรื้อรังระยะสุดท้าย และเมื่อระดับความดันโลหิตตัวล่างมากกว่า 90 มิลลิเมตรปรอทจะเพิ่มความเสี่ยงต่อการเกิดโรคไตเรื้อรังระยะสุดท้าย1 ดังนั้น การวินิจฉัย หาสาเหตุ ประเมินความรุนแรงโรค และการรักษาอย่างเหมาะสมจึงเป็นสิ่งที่สำคัญ
กลไกการเกิดความดันโลหิตสูงในผู้ป่วยโรคไตเรื้อรัง
ไตเป็นอวัยวะสำคัญในการขับโซเดียมออกทางปัสสาวะ ภาวะปกติเมื่อรับประทานโซเดียมเพิ่มขึ้นจะมีการเพิ่มความดันโลหิตแล้วเกิดการปรับตัวที่เรียกว่า pressure natriuresis เพื่อขับโซเดียมเพิ่มขึ้นทางปัสสาวะทำให้ความดันโลหิตปกติ กรณีผู้ป่วยโรคไตเรื้อรังจะมีความสามารถขับโซเดียมลดลงเมื่อรับประทานโซเดียมเพิ่มขึ้น จึงทำให้เกิดความดันโลหิตสูงกลุ่มที่เรียกว่า salt-sensitive hypertension

รูปที่ 1
ระยะแรกของความดันโลหิตสูง เริ่มจากหลอดเลือดไตหดตัว (renal vasoconstriction) จากการกระตุ้น renal sympathetic nerves, renin angiotensin aldosterone system (RAAS), oxidative stress และ endothelin-1 เพิ่มขึ้นภายในไต และมีลดการสร้าง nitric oxide (NO) ภายในหลอดเลือดไตทำให้ภาวะ endothelial cell dysfunction มากขึ้น ทำให้เกิดความดันโลหิตสูงแบบ salt resistant และ renin dependent โดยที่การทำงานของไตปกติ ระยะต่อมาเกิดพยาธิสภาพของหลอดเลือดภายในไต (renal arteriolosclerosis) การอักเสบของท่อไต (tubulointerstitial inflammation) และการขาดเลือดของท่อไต (ischemic tubular injury) ทำให้เกิดความดันโลหิตสูงแบบ salt-sensitive, volume-dependent และ renal-dependent pathway
คำจำกัดความของความดันโลหิตสูง
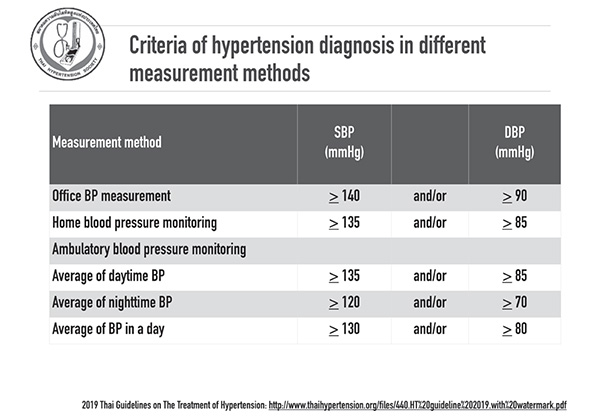
คำจำกัดความของความดันโลหิตสูง คือ systolic blood pressure (SBP) มากกว่าหรือเท่ากับ 140 มิลลิเมตรปรอท หรือ diastolic blood pressure (DBP) มากกว่าหรือเท่ากับ 90 มิลลิเมตรปรอท และตามสมาคมความดันโลหิตสูงของประเทศไทย ปี พ.ศ. 2562 แบ่งความรุนแรงของโรค แสดงในรูปที่ 1 และนิยามความดันโลหิตสูงจากการวัดความดันโลหิตด้วยเครื่องชนิดติดตัวพร้อมวัดอัตโนมัติ (ambulatory blood pressure monitoring, ABPM) และเครื่องชนิดพกพาที่บ้าน (self หรือ home blood pressure monitoring, HBPM) ในรูปที่ 2
 รูปที่ 2
รูปที่ 2
การวัดความดันโลหิตด้วย ABPM ช่วยในการตรวจหาผู้ป่วยที่เป็น whitecoat hypertension และ masked hypertension และการวัดความดันโลหิตด้วย ABPM และ HBPM สัมพันธ์กับการเกิดโรคหัวใจและหลอดเลือด และการเสียชีวิตในอนาคตได้ดีกว่าระดับความดันโลหิตในสถานพยาบาล โดยระดับความดันโลหิตในช่วงกลางคืนควรลดลงอย่างน้อยร้อยละ 10 เมื่อเทียบกับความดันโลหิตในช่วงกลางวัน ผู้ป่วยที่มีการลดลงของความดันโลหิตในช่วงกลางคืนน้อยกว่าร้อยละ 10 มีความเสี่ยงต่อการเกิดโรคหัวใจและหลอดเลือดระดับแอลบูมินในปัสสาวะ และโรคไตเรื้อรังระยะสุดท้ายมากกว่าผู้ป่วยที่ตรวจพบการลดลงของความดันโลหิตในช่วงกลางคืน และระดับความดันโลหิตในช่วงกลางคืนสัมพันธ์กับการเกิดโรคหัวใจและหลอดเลือดดีกว่าความดันโลหิตในช่วงกลางวัน2 ปัจจุบันจึงแนะนำให้ใช้การวัดความดันโลหิตที่บ้านในการติดตามผลการรักษาผู้ป่วยโรคความดันโลหิตสูง
 รูปที่ 3
รูปที่ 3
สาเหตุของความดันโลหิตสูง
ประมาณร้อยละ 80 – 95 ของผู้ป่วยความดันโลหิตสูงไม่ทราบสาเหตุ หรือเรียกว่า essential hypertension เชื่อว่าเป็นผลจากปัจจัยทางสิ่งแวดล้อม และทางกรรมพันธุ์ภายในครอบครัว ดังแสดงตามกลไกการเกิดความดันโลหิตสูง โดยมีอุบัติการณ์ของโรคพบเพิ่มขึ้นตามอายุ และประมาณร้อยละ 5 – 20 สามารถตรวจพบสาเหตุของความดันโลหิตสูง หรือเรียกว่า secondary hypertension ดังแสดงในรูปที่ 3
การประเมินผู้ป่วยความดันโลหิตสูง
การซักประวัติ การตรวจร่างกาย และการตรวจทางห้องปฏิบัติการเพื่อยืนยันว่าเป็นโรคความดันโลหิตสูงจริง ประเมินความรุนแรงของโรค ตรวจหา target organ damage จากความดันโลหิตสูง ได้แก่ กล้ามเนื้อหัวใจโต (left ventricular hypertrophy, LVH) ความดันโลหิตสูงขึ้นจอประสาทตา (hypertensive retinopathy) โรคหลอดเลือดแดงแข็ง และการตรวจพบแอลบูมินในปัสสาวะ เป็นต้น ตรวจหาโรคที่เพิ่มความเสี่ยงต่อการเกิดโรคหัวใจและหลอดเลือด เช่น โรคเบาหวาน โรคไขมันในเลือดสูง และโรคไต และสุดท้ายเพื่อตรวจหาโรคความดันโลหิตสูงที่มีสาเหตุดังกล่าวข้างต้น โดยการตรวจทางห้องปฏิบัติการเบื้องต้นตามคำแนะนำของสมาคมความดันโลหิตสูงของประเทศไทยในผู้ป่วยความดันโลหิตสูงทุกรายมีดังนี้
- ระดับฮีโมโกลบิน และความเข้มข้นเลือด
- ระดับน้ำตาลในเลือดขณะอดอาหาร และน้ำตาลสะสมในเลือด
- ระดับไขมันในเลือด
- คลื่นไฟฟ้าหัวใจ
- ระดับครีเอทินินในเลือด และประเมินอัตราการกรองของไต
- ระดับโซเดียม โพแทสเซียม และยูริกในเลือด
- การทำงานของตับ
- ตรวจปัสสาวะ และการตรวจโปรตีนในปัสสาวะ หรือแอลบูมินในปัสสาวะ
- ภาพรังสีทรวงอก
สำหรับการตรวจเพิ่มเติมอื่น ๆ พิจารณาเป็นราย ๆ ไป ตามอาการ อาการแสดงของผู้ป่วย และการตรวจสืบค้นเพิ่มเติม เพื่อประเมินอวัยวะที่ถูกผลกระทบจากความดันโลหิตสูง เช่น คลื่นเสียงสะท้อนความถี่สูงหัวใจ (echocardiogram) ในผู้ป่วยที่มีความผิดปกติของคลื่นไฟฟ้าหัวใจ หรือมีอาการแสดงของการทำงานของหัวใจห้องล่างซ้ายผิดปกติ ประเมิน carotid intima media thickness (CIMT) คลื่นเสียงสะท้อนไต และดอปเปอร์ (doppler) ในผู้ป่วยที่การทำงานของไตผิดปกติ มีแอลบูมินในปัสสาวะ หรือสงสัยโรคความดันโลหิตสูงแบบทุติยภูมิ และภาพรังสีคอมพิวเตอร์ หรือคลื่นแม่เหล็กไฟฟ้าสมองในผู้ป่วยที่มีอาการทางสมอง หรือมีความผิดปกติของความจำ
อาการแสดงทางไตจากความดันโลหิตสูง
ส่วนใหญ่ของผู้ป่วยความดันโลหิตสูงระยะแรกจะมีการทำงานของไตปกติและปัสสาวะปกติ แต่อย่างไรก็ตาม เมื่อตรวจพยาธิสภาพไตจะพบรอยโรคที่หลอดเลือดเกิดขึ้นเป็น arteriolosclerosis และ vascular hyalinosis หากควบคุมความดันโลหิตไม่ดีเป็นระยะนานจะเริ่มตรวจพบแอลบูมินในปัสสาวะ หรือโปรตีนในปัสสาวะ ซึ่งส่วนใหญ่พบประมาณ 1 – 2 กรัมต่อวัน สุดท้ายทำให้การทำงานของไตลดลงตามจากการเกิดพยาธิสภาพของหลอดเลือดรุนแรงมากขึ้น ร่วมกับพบ tubulointerstitial inflammation/fibrosis, glomerular ischemic shrinking, glomerular sclerosis และ focal segmental glomerulosclerosis ได้ ดังนั้น การตรวจแอลบูมินในปัสสาวะจึงเป็นหลักฐานสำคัญของการเกิดพยาธิสภาพของหลอดเลือดไตในผู้ป่วยความดันโลหิตสูง
เป้าหมายของระดับความดันโลหิต
เป้าหมายของระดับความดันโลหิตส่วนใหญ่แนะนำลดความดันโลหิต น้อยกว่า 140/90 มิลลิเมตรปรอท และหากผู้ป่วยทนต่อการรักษาได้ดีสามารถปรับการรักษาจนระดับความดันโลหิตน้อยกว่า 130/80 มิลลิเมตรปรอท หรือประมาณ SBP 120-129 มิลลิเมตรปรอท เนื่องจากมีการศึกษา SPRINT trial โดยร้อยละ 28 ของผู้ป่วยเป็นผู้ป่วยโรคไตเรื้อรังร่วมด้วย พบว่า การควบคุมความดันโลหิตอย่างเข้มงวด คือ ความดันโลหิตตัวบนน้อยกว่า 120 มิลลิเมตรปรอท เทียบกับ 140 มิลลิเมตรปรอท สามารถลดอัตราการเกิดโรคหัวใจและหลอดเลือดโดยรวมในกลุ่มที่มีโรคไตเรื้อรังได้เช่นกัน3 ดังนั้น การควบคุมระดับความดันโลหิตอย่างเข้มงวดจึงมีประโยชน์ในผู้ป่วยโรคไตเรื้อรังเพื่อป้องกันการเกิดโรคหัวใจและหลอดเลือด แต่อย่างไรก็ตาม การควบคุมระดับความดันโลหิตอย่างเข้มงวดเพิ่มอัตราการเกิดความดันโลหิตต่ำ หน้ามืดเป็นลม เกลือแร่ในเลือดผิดปกติ และไตวายเฉียบพลันเพิ่มมากขึ้นจึงจำเป็นต้องติดตามการรักษาอย่างใกล้ชิดในช่วงแรกของการปรับลดความดันโลหิต
เป้าหมายของระดับความดันโลหิตของกลุ่มผู้ป่วยสูงอายุมากกว่า 65 ปี แนะนำลดความดันโลหิต ประมาณ SBP 130 – 139 มิลลิเมตรปรอท เนื่องจากหากให้ยาเพื่อลดความดันโลหิตลงมากเกินไปอาจมีผลเสียมาก ดังนั้น ต้องพึงระวังผลข้างเคียงจากการลดความดันโลหิตแบบเข้มงวด โดยเฉพาะกลุ่มผู้ป่วยสูงอายุจากการเพิ่มอัตราการล้ม ความผิดปกติของเกลือแร่ในเลือด และการเกิดไตวายเฉียบพลันในช่วงแรกของการรักษาได้จากการลดความดันโลหิตอย่างรวดเร็ว
หลักฐานการควบคุมความดันโลหิตในโรคไตเรื้อรัง
จากการศึกษา AASK Collaborative Research Group ถึงผลของการควบคุมความดันโลหิตอย่างเข้มงวด คือ ความดันโลหิตตัวบนน้อยกว่า 130 มิลลิเมตรปรอท เทียบกับ 140 มิลลิเมตรปรอท สามารถลดอัตราการเกิดไตเรื้อรังระยะสุดท้าย หรือการเกิด doubling of plasma creatinine เฉพาะในกลุ่มที่มีโรคไตเรื้อรังที่มีโปรตีนในปัสสาวะมากกว่า 0.22 กรัมต่อกรัม ครีแอทินิน4 และจากการศึกษา Modification of Diet in Renal Disease Study (MDRD) ถึงผลของการควบคุมความดันโลหิตอย่างเข้มงวด คือ ความดันโลหิต mean arterial blood pressure น้อยกว่า 92 มิลลิเมตรปรอทเทียบกับ 107 มิลลิเมตรปรอท สามารถลดอัตราการเกิดไตเรื้อรังระยะสุดท้ายร้อยละ 32 (HR 0.68,95% CI, 0.57 to 0.82; P < 0.001) ในผู้ป่วยโรคไตเรื้อรังที่มีการทำงานของไต 13 – 55 มล./นาที/1.73 ตารางเมตร5 และการศึกษาแบบ meta-analyses และ systematic reviews พบว่า การควบคุมความดันโลหิตอย่างเข้มงวดสามารถชะลอการเสื่อมของไตได้ในในผู้ป่วยที่มีแอลบูมินในปัสสาวะ6
การรักษาความดันโลหิตสูง
การรักษาความดันโลหิตสูงควรเริ่มจากการปรับเปลี่ยนพฤติกรรมชีวิต ได้แก่ การจำกัดเกลือในอาหารน้อยกว่า 5 กรัม/วัน การจำกัดปริมาณเครื่องดื่มแอลกอฮอล์ โดยสำหรับผู้ชาย ไม่เกิน 2 ดื่มมาตรฐานต่อวัน และผู้หญิงไม่เกิน 1 ดื่มมาตรฐานต่อวัน ลดน้ำหนักในผู้ที่มีภาวะน้ำหนักเกิน หรืออ้วน การออกกำลังกายแบบแอโรบิกอย่างสม่ำเสมอ การรับประทานอาหารที่มีผักผลไม้เพิ่มขึ้น และลดอาหารที่มีไขมันอิ่มตัวสูง และงดสูบบุหรี่ เป็นต้น
การรักษาความดันโลหิตสูงด้วยยาลดความดันโลหิตเพื่อการลดโอกาสเสี่ยงของโรคหัวใจและหลอดเลือด โรคหลอดเลือดสมอง โรคไต และอัตราการเสียชีวิตควรเริ่มหลังการปรับเปลี่ยนการดำเนินชีวิตแล้วไม่สามารถควบคุมระดับความดันโลหิตได้ตามเป้าหมาย และควรพิจารณาเริ่มยาลดความดันโลหิตตามความเสี่ยงต่อการเกิดโรคหัวใจและหลอดเลือดดังแสดงในรูปที่ 4
 รูปที่ 4
รูปที่ 4
การเลือกใช้ยาลดความดันโลหิตสูง
ยารักษาความดันโลหิตสูงที่สำคัญ มีอยู่ 5 กลุ่มหลัก คือ angiotensin converting enzyme inhibitor (ACEI), angiotensin receptor blockers (ARB), beta-blocker (BB), calcium-channel blockers (CCB) และยาขับปัสสาวะ (thiazide และยาขับปัสสาวะที่ใกล้เคียงกับ thiazide ได้แก่ chlorthalidone และ indapamide)
การเลือกใช้ยาชนิดใดชนิดหนึ่งจาก 5 กลุ่มนี้ จะให้ประสิทธิภาพในการลดความดันโลหิต และลดอัตราการเกิดโรคทางระบบหัวใจและหลอดเลือดได้ใกล้เคียงกัน ดังนั้น หากจะเลือกยาเริ่มต้นในการรักษาความดันโลหิตสูงเพียงชนิดเดียวก็สามารถเลือกจากกลุ่มใดก็ได้ตามความเหมาะสม กรณีที่มีโรคร่วมแล้ว พบว่า ยาลดความดันโลหิตบางกลุ่มได้ประโยชน์มากขึ้นกว่ายาลดความดันโลหิตกลุ่มอื่น ๆ ซึ่งเรียกว่า compelling indications
ยาลดความดันโลหิตสูงในผู้ป่วยโรคไตเรื้อรัง
- ผู้ป่วยโรคไตเรื้อรังที่มีโปรตีนในปัสสาวะ หรือแอลบูมินในปัสสาวะมากกว่า 300 มก./วัน ควรเลือกใช้ ACEI หรือ ARB เป็นกลุ่มแรก เนื่องจากยาสามารถลด intraglomerular pressure จากการขยาย efferent arteriole มากกว่า afferent arteriole จึงลดภาวะโปรตีนรั่วในปัสสาวะ ชะลอการเสื่อมของไตในผู้ป่วยโรคไตเรื้อรังได้7
.
ACEI สามารถลดโปรตีนในปัสสาวะ และชะลอการเสื่อมของไตในผู้ป่วยได้ โดยเฉพาะสามารถลดอัตราการเกิดไตเรื้อรังระยะสุดท้ายในผู้ป่วยเบาหวานชนิดที่ 1 ได้8 สำหรับ ARB จากสองการศึกษาหลัก คือ Irbesartan Diabetic kidney disease Trial (IDNT)9 และ Reduction of End point in NIDDM with the Angiotensin II Antagonist Losartan (RENAAL) trial10 ศึกษาผลของยา irbesartan และ losartan ในผู้ป่วยโรคไตจากเบาหวานระยะแมคโครแอลบูมินในปัสสาวะ ติดตามเป็นระยะเวลา 2.6 – 3.4 ปี พบว่า ยากลุ่ม ARB สามารถลดอัตราการเกิดโรคไตเรื้อรังระยะสุดท้ายถึงร้อยละ 23 – 28 เมื่อเทียบกับยาลดความดันโลหิตกลุ่มอื่น ๆ โดยที่ระดับความดันโลหิตของผู้ป่วยทั้งสองกลุ่มไม่มีความแตกต่างกัน จึงเป็นหลักฐานสำคัญที่แนะนำให้เลือกใช้ยา ACEI/ARB ในการชะลอการเสื่อมของโรคไตจากเบาหวานที่สำคัญอ้างอิงจากการศึกษาแบบ meta-analysis ในผู้ป่วยโรคไตเรื้อรัง จำนวน 564,768 ราย พบว่า ACEI/ARB สามารถลดโอกาสเกิดโรคไตเรื้อรังระยะท้ายประมาณร้อยละ 30 – 40 และลดการเกิดโรคหลอดเลือดหัวใจประมาณร้อยละ 18 – 2411 จึงเป็นหลักฐานสำคัญที่แนะนำให้เลือกใช้ยา ACEI/ARB ในการชะลอการเสื่อมของโรคไต และป้องกันการเกิดโรคหลอดเลือดหัวใจ
.
ACEI ร่วมกับ ARB สามารถเพิ่มประสิทธิภาพในการลดโปรตีนในปัสสาวะในผู้ป่วยโรคไตจากเบาหวาน แต่พบว่า ยา ACEI ร่วมกับ ARB เพิ่ม อัตราการเกิดไตวายเฉียบพลัน การบำบัดทนแทนทางไต โพแทสเซียมในเลือดสูง และความดันโลหิตต่ำมากกว่ากลุ่มที่ได้รับ ACEI หรือ ARB อย่างเดียว12 และจากการศึกษา Veterans Affairs Nephropathy in Diabetes (VA-NEPHRON-D) study ในผู้ป่วยเบาหวาน จำนวน 1,448 ราย ให้ผลเช่นเดียวกันว่า ยา ACEI ร่วมกับ ARB เพิ่มอัตราการเกิดไตวายเฉียบพลัน และโพแทสเซียมในเลือดสูงมากกว่ากลุ่มที่ได้รับ ACEI หรือ ARB อย่างเดียว และการศึกษานี้จำเป็นต้องยุติก่อนกำหนด เนื่องจากผลข้างเคียงของการรักษาดังกล่าว13 ดังนั้น ปัจจุบันจึงไม่แนะนำให้ยา ACEI ร่วมกับ ARB ในการควบคุมความดันโลหิตสูง และชะลอการเสื่อมของไต..
.
เห็นได้ว่า ผู้ป่วยโรคไตจากเบาหวานควรเลือกใช้ยากลุ่ม ACEI หรือ ARB เป็นกลุ่มแรก ยกเว้นผู้ป่วยมีข้อห้ามของการใช้ยา คือ ประวัติจากการใช้ยา ACEI หรือ ARB เกิด angioedema ภาวะโพแทสเซียมในเลือดสูง ภาวะหลอดเลือดแดงของไตตีบสองข้าง ภาวะไตวายเฉียบพลันและการตั้งครรภ์ เนื่องจากการใช้ยา ACEI หรือ ARB ในช่วงไตรมาสแรกของการตั้งครรภ์เพิ่มความเสี่ยงต่อการเกิดความผิดปกติของหัวใจและหลอดเลือด คือ atrial septal defect หรือ ventricular septal defect และความเสี่ยงต่อการเกิดความผิดปกติของระบบประสาท คือ spina bifida หรือ microcephaly การใช้ยา ACEI หรือ ARB ในช่วงไตรมาสสอง และสามของการตั้งครรภ์เพิ่มความเสี่ยงต่อการเกิดความผิดปกติทางไต คือ renal dysgenesis, oligohydramnios และเพิ่มอัตราการเสียชีวิตของทารกในครรภ์..
เมื่อเริ่มรักษาหรือปรับขนาดยา ACEI หรือ ARB เป็นระยะเวลา 4 – 8 สัปดาห์ มีระดับครีแอทินินในเลือดเพิ่มขึ้นมากกว่าหรือเท่ากับร้อยละ 3014 ควรหยุดยา และหาสาเหตุของการเพิ่มขึ้นของระดับครีแอทินินในเลือด ได้แก่ ภาวะหลอดเลือดแดงของไตตีบสองข้าง ภาวะขาดสารน้ำต่าง ๆ หรือยาที่ใช้ร่วม เช่น NSIADs เป็นต้น และสุดท้ายควรใช้ยาอย่างระมัดระวังในผู้ป่วยที่มีระดับครีแอทินินในเลือดมากกว่า 3.0 มก./ดล.
.
- ผู้ป่วยโรคไตเรื้อรังที่ไม่มีโปรตีนในปัสสาวะ หรือแอลบูมินในปัสสาวะน้อยกว่า 300 มก./วัน สามารถเลือกใช้ยาลดความดันโลหิตกลุ่มใดก็ได้ เช่น ACEI, ARB, CCB หรือ diuretic บทบาทของการเลือกใช้ยา ACEI/ARB ในผู้ป่วยโรคไตเรื้อรังที่มีโปรตีนรั่วในปัสสาวะน้อยกว่า 500 มก./วัน ในการชะลอการเสื่อมของโรคไต ไม่แตกต่างกับยา CCB, diuretic และ BB15 ดังนั้น ผู้ป่วยโรคไตเรื้อรังที่แอลบูมินในปัสสาวะน้อยกว่า 300 มก./วัน สามารถเลือกใช้ยาลดความดันโลหิตกลุ่มใดก็ได้ เช่น ACEI, ARB, CCB หรือ diuretic สำหรับการเลือกใช้ยาขับปัสสาวะในผู้ป่วยโรคไตเรื้อรัง ควรเลือกใช้ยาขับปัสสาวะกลุ่ม thiazide ในผู้ป่วยไตเรื้อรังที่มีการทำงานของไตมากกว่า หรือเท่ากับ 30 มล./นาที/1.73 ตารางเมตร ส่วนยาขับปัสสาวะ loop diuretic เลือกใช้ในผู้ป่วยไตเรื้อรังที่มีการทำงานของไตน้อยกว่า 30 มล./นาที/1.73 ตารางเมตร
การพิจารณายาลดความดันโลหิตร่วมกัน
จากการศึกษาต่าง ๆ ในผู้ป่วยโรคความดันโลหิตสูง รวมทั้งผู้ป่วยเบาหวาน และโรคไตเรื้อรัง ส่วนใหญ่แล้ว จำเป็นต้องใช้ยาลดความดันโลหิตอย่างน้อย 2 กลุ่ม เพื่อควบคุมความดันโลหิตให้ได้ตามเป้าหมาย โดยหลักการพิจารณายาลดความดันโลหิตร่วมกัน คือ เลือกใช้ยาลดความดันโลหิต 2 ชนิดที่สามารถเสริมฤทธิ์กันได้ดี ส่วนใหญ่แนะนำกลุ่ม ACEI หรือ ARB ร่วมกับ CCB หรือ diuretic เป็นหลัก นอกจากนี้ มีการศึกษาเพิ่มเติมจาก ACCOMPLISH study พบว่า การใช้ยากลุ่ม ACEI ร่วมกับ CCB สามารถลดอัตราการเจ็บป่วย และเสียชีวิตจากโรคหัวใจและหลอดเลือดประมาณร้อยละ 20 เมื่อเทียบกับการใช้ยากลุ่ม ACEI ร่วมกับ diuretic16 และเมื่อวิเคราะห์เพิ่มเติมถึงผลของยาต่อการเกิดโรคไตเรื้อรังพบเช่นเดียวกันว่า การใช้ยากลุ่มACEI ร่วมกับ CCB สามารถลดเกิดโรคไตเรื้อรังเท่ากับ 0.52 (95% CI 0.41-0.65)17 ต่อมามีการศึกษาแบบ meta-analysis ในผู้ป่วยความดันโลหิตสูงจำนวน 20,451 ราย ยืนยันว่ายากลุ่ม RAAS blocker ร่วมกับ CCB สามารถลดอัตราการเจ็บป่วย และเสียชีวิตจากโรคหัวใจและหลอดเลือดประมาณร้อยละ 20 เมื่อเทียบกับการใช้ยากลุ่ม RAAS blocker ร่วมกับยากลุ่มอื่น ๆ18 จึงเห็นได้ว่าการใช้ยา กลุ่ม ACEI หรือ ARB ร่วมกับ CCB เป็นทางเลือกหลักของการใช้ยาลดความดันโลหิตร่วมกัน
หากใช้ยา 2 ชนิดแล้วยังไม่สามารถควบคุมความดันโลหิตได้ ควรใช้ยารักษาความดันโลหิต 3 ชนิด โดยหนึ่งใน 3 ชนิดควรจะเป็นยาขับปัสสาวะ และหากใช้ยา 3 ชนิดแล้วยังไม่สามารถควบคุมความดันโลหิตได้เรียกว่า resistant hypertension ควรเพิ่ม spironolactone, BB และ alpha-blocker ตามลำดับ19 โดยผู้ป่วย resistant hypertension พบได้ประมาณร้อยละ 13 – 16 ของผู้ป่วยความดันโลหิตสูงทั้งหมด20 โดยส่วนใหญ่พบในผู้ป่วยสูงอายุ อ้วน ความดันโลหิตที่ควบคุมไม่ดี โรคไตเรื้อรัง เบาหวาน โรคความดันโลหิตสูงที่มีสาเหตุ และพฤติกรรมชีวิตไม่เหมาะสม โดยมีแนวทางการประเมินและรักษา resistant hypertension ดังรูปที่ 5
 รูปที่ 5
รูปที่ 5
สรุป
ความดันโลหิตสูงเป็นโรคที่พบบ่อยประมาณร้อยละ 80 – 95 ของผู้ป่วยความดันโลหิตสูงไม่ทราบสาเหตุ และประมาณร้อยละ 5 – 20 สามารถตรวจพบสาเหตุของความดันโลหิตสูง หรือเรียกว่า secondary hypertension ควรได้รับการตรวจประเมิน การซักประวัติ การตรวจร่างกาย และการตรวจทางห้องปฏิบัติการเพื่อยืนยันว่าเป็นโรคความดันโลหิตสูงจริง ประเมินความรุนแรงของโรค ตรวจหา target organ damage จากความดันโลหิตสูง และตรวจหาโรคความดันโลหิตสูงที่มีสาเหตุในผู้ป่วยในกลุ่มที่ควรสงสัย secondary hypertension แล้วรักษาตามสาเหตุของโรค ควบคุมระดับความดันโลหิตอย่างเหมาะสม โดยเริ่มจากการปรับเปลี่ยนการดำเนินชีวิตและการเลือกยาลดความดันโลหิตตามข้อบ่งชี้ และติดตามการรักษา อย่างสม่ำเสมอในผู้ป่วยทุกราย เพื่อปรับความดันโลหิตสูงตามเป้าหมายในผู้ป่วยแต่ละราย และติดตามผลข้างเคียงของการรักษา
เอกสารอ้างอิง
- Peralta CA, Norris KC, Li S, et al. Blood pressure components and end-stage renal disease in persons with chronic kidney disease: the Kidney Early Evaluation Program (KEEP). Arch Intern Med 2012;172:41-7.
- Brotman DJ, Davidson MB, Boumitri M, Vidt DG. Impaired diurnal blood pressure variation and all-cause mortality. Am J Hypertens 2008;21:92-7.
- Cheung AK, Rahman M, Reboussin DM, et al. Effects of Intensive BP Control in CKD. J Am Soc Nephrol 2017;28:2812-23.
- Appel LJ, Wright JT, Jr., Greene T, et al. Intensive blood-pressure control in hypertensive chronic kidney disease. N Engl J Med 2010;363:918-29.
- Sarnak MJ, Greene T, Wang X, et al. The effect of a lower target blood pressure on the progression of kidney disease: long-term follow-up of the modification of diet in renal disease study. Ann Intern Med 2005;142:342-51.
- Upadhyay A, Earley A, Haynes SM, Uhlig K. Systematic review: blood pressure target in chronic kidney disease and proteinuria as an effect modifier. Ann Intern Med 2011;154:541-8.
- Hostetter TH. Prevention of end-stage renal disease due to type 2 diabetes. N Engl J Med 2001;345:910-2.
- Parving HH, Rossing P. The use of antihypertensive agents in prevention and treatment of diabetic nephropathy. Curr Opin Nephrol Hypertens 1994;3:292-300.
- Lewis EJ, Hunsicker LG, Clarke WR, et al. Renoprotective effect of the angiotensin-receptor antagonist irbesartan in patients with nephropathy due to type 2 diabetes. N Engl J Med 2001;345:851-60.
- Brenner BM, Cooper ME, de Zeeuw D, et al. Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy. N Engl J Med 2001;345:861-9.
- Xie X, Liu Y, Perkovic V, et al. Renin-Angiotensin System Inhibitors and Kidney and Cardiovascular Outcomes in Patients With CKD: A Bayesian Network Meta-analysis of Randomized Clinical Trials. Am J Kidney Dis 2016;67:728-41.
- Investigators O, Yusuf S, Teo KK, et al. Telmisartan, ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008;358:1547-59.
- Fried LF, Emanuele N, Zhang JH, et al. Combined angiotensin inhibition for the treatment of diabetic nephropathy. N Engl J Med 2013;369:1892-903.
- Holtkamp FA, de Zeeuw D, Thomas MC, et al. An acute fall in estimated glomerular filtration rate during treatment with losartan predicts a slower decrease in longterm renal function. Kidney Int 2011;80:282-7.
- Kent DM, Jafar TH, Hayward RA, et al. Progression risk, urinary protein excretion, and treatment effects of angiotensin-converting enzyme inhibitors in nondiabetic kidney disease. J Am Soc Nephrol 2007;18:1959-65.
- Jamerson K, Weber MA, Bakris GL, et al. Benazepril plus amlodipine or hydrochlorothiazide for hypertension in high-risk patients. N Engl J Med 2008;359:2417-28.
- Bakris GL, Sarafidis PA, Weir MR, et al. Renal outcomes with different fixed-dose combination therapies in patients with hypertension at high risk for cardiovascular events (ACCOMPLISH): a prespecified secondary analysis of a randomised controlled trial. Lancet 2010;375:1173-81.
- Chi C, Tai C, Bai B, et al. Angiotensin System Blockade Combined With Calcium Channel Blockers Is Superior to Other Combinations in Cardiovascular Protection With Similar Blood Pressure Reduction: A Meta-Analysis in 20,451 Hypertensive Patients. J Clin Hypertens (Greenwich) 2016;18:801-8.
- Whelton PK, Carey RM, Aronow WS, et al. 2017 ACC/AHA/AAPA/ABC/ACPM/AGS/APhA/ASH/ ASPC/NMA/PCNA Guideline for the Prevention, Detection, Evaluation, and Management of High Blood Pressure in Adults: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Hypertension 2018;71:e13-e115.
- Achelrod D, Wenzel U, Frey S. Systematic review and meta-analysis of the prevalence of resistant hypertension in treated hypertensive populations. Am J Hypertens 2015;28:355-61.





