 นพ. วิภาช กิตติวีรวงศ์
นพ. วิภาช กิตติวีรวงศ์
อนุสาขาวิชาโรคไต สาขาวิชาอายุรศาสตร์
คณะแพทยศาสตร์ มหาวิทยาลัยขอนแก่น
 รศ. นพ. กิตติ์รวี กฤษฏิ์เมธาภาคย์
รศ. นพ. กิตติ์รวี กฤษฏิ์เมธาภาคย์
อนุสาขาวิชาโรคไต สาขาวิชาอายุรศาสตร์
คณะแพทยศาสตร์ มหาวิทยาลัยขอนแก่น
ภาวะหัวใจล้มเหลว (heart failure, HF) และภาวะไตวาย มักเกิดร่วมกันได้บ่อย โดย cardiorenal syndrome (CRS) หมายถึง ความผิดปกติที่การทำงานของหัวใจหรือไตลดลง ส่งผลให้อีกระบบทำงานแย่ลงตาม1 CRS จำแนกออกเป็น 5 ชนิด (ตารางที่ 1) ตามอวัยวะที่เป็นสาเหตุหลักและลักษณะการดำเนินโรค (เฉียบพลันหรือเรื้อรัง) กลไกการเกิด CRS เกี่ยวข้องกับ hemodynamic mechanism, neurohormonal activation, inflammation และ endothelial dysfunction (รูปที่ 1)
ตารางที่ 1 การจำแนกชนิดของ cardiorenal syndrome คำย่อ AHF, acute heart failure; AKI, acute kidney injury; CHF, chronic heart failure; CKD, chronic kidney disease
คำย่อ AHF, acute heart failure; AKI, acute kidney injury; CHF, chronic heart failure; CKD, chronic kidney disease
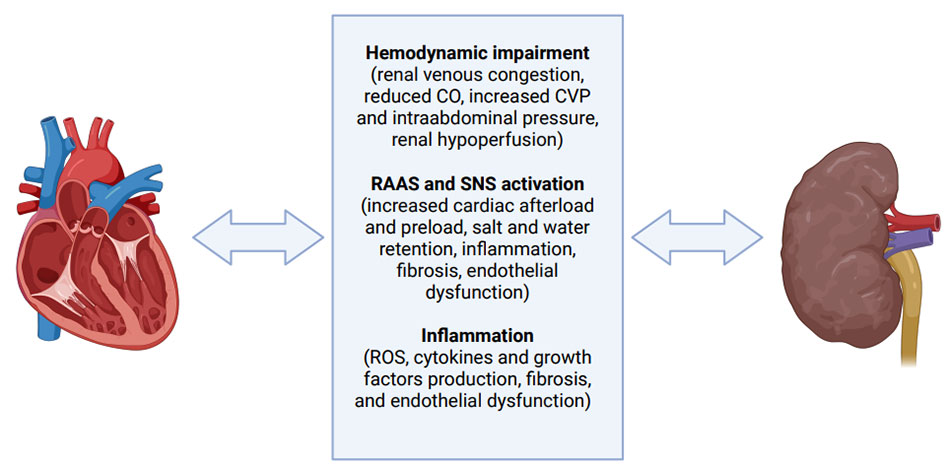 รูปที่ 1 แสดงพยาธิสรีรวิทยาของการเกิด cardiorenal syndrome2
รูปที่ 1 แสดงพยาธิสรีรวิทยาของการเกิด cardiorenal syndrome2
คำย่อ CO, cardiac output; CVP, central venous pressure; RAAS, renin-angiotensin-aldosterone system; ROS, reactive oxygen species; SNS, sympathetic nervous system
การวินิจฉัย
- Cardiac biomarkers3
- Natriuretic peptides ได้แก่ B-type natriuretic peptide (BNP) และ N-terminal pro-B-type natriuretic peptide (NT-proBNP) เป็น biomarkers ที่ได้รับการยอมรับอย่างแพร่หลายในการวินิจฉัยภาวะ HF ทั้งชนิดเฉียบพลันและเรื้อรัง อย่างไรก็ตาม ระดับของ natriuretic peptides มักสูงขึ้นในผู้ป่วยที่มีภาวะไตวายเช่นกัน
- Cardiac troponins พบว่าในผู้ป่วย HF หากมีระดับ troponin I ในระดับสูงแม้ได้รับการรักษา มีความสัมพันธ์กับภาวะ congestion อย่างไรก็ตาม การใช้ cardiac troponins ในการประเมิน congestion ในผู้ป่วย CRS ยังจำเป็นต้องมีการศึกษาต่อเพิ่มเติม
- Biomarkers อื่น ๆ เช่น galectin-3, platelet-derived growth factor (PDGF), soluble VEGF receptor-1 (sFlt-1), soluble suppressor of tumorigenicity-2 (sST2) และ myeloperoxidase (MPO) อยู่ระหว่างการศึกษาความสัมพันธ์กับการเกิดและพยากรณ์โรคใน CRS
- Renal biomarkers ช่วยในการวินิจฉัยและพยากรณ์ภาวะ AKI และ CRS เช่น
- Neutrophil gelatinase-associated lipocalin (NGAL) เป็นโปรตีนที่สร้างจาก renal tubule และจะหลั่งเพิ่มขึ้นเมื่อมีการบาดเจ็บของ renal tubule ในผู้ป่วย AKI ระดับ NGAL ในเลือดและปัสสาวะจะเพิ่มขึ้นภายใน 2 ชั่วโมงแรก จึงใช้เป็น early biomarker ของ AKI ได้ ผู้ป่วย HF ที่ได้รับยาขับปัสสาวะเพื่อลด congestion อาจมีระดับ serum creatinine สูงขึ้น โดยที่ระดับ urine NGAL ปกติ ซึ่งบ่งชี้ถึง hemodynamic effect
- Tissue inhibitor of metalloproteinase-2 (TIMP-2) และ Insulin-like growth factor-binding protein 7 (IGFBP7) โปรตีนทั้ง 2 ชนิดถูกสร้างจาก renal tubule ภายใต้ภาวะอักเสบหรือ oxidative stress โดยระดับของโปรตีนเหล่านี้ในปัสสาวะจะเพิ่มขึ้นตั้งแต่ระยะก่อนที่เซลล์จะเกิดการบาดเจ็บ มีการศึกษาพบว่าค่าผลคูณ [TIMP-2] × [IGFBP7] สามารถทำนายการเกิด AKI ระยะที่ 2-3 ในผู้ป่วย acute HF ได้4
- Biomarkers อื่น ๆ เช่น urine interleukin-18, liver fatty acid-binding protein (L-FABP), fibroblast growth factor 23 (FGF23), proenkephalin A, urine angiotensinogen กำลังอยู่ระหว่างการศึกษาถึงความสัมพันธ์กับการเกิดและพยากรณ์โรคในภาวะ CRS
- การประเมินทางรังสีวิทยา
- Echocardiography และ Cardiac magnetic resonance imaging (MRI) ใช้ประเมินโครงสร้างและการทำงานของหัวใจในภาวะ CRS อย่างละเอียด
- การประเมินภาวะ venous congestion ซึ่งเป็นกลไกสำคัญของ Type 1 CRS สามารถทำได้หลายวิธี เช่น:
- Echocardiography
- Lung ultrasound
- Venous excess ultrasound score (VExUS) โดย VExUS ใช้การตรวจ flow ของหลอดเลือดดำต่าง ๆ ได้แก่ intrarenal vein, portal vein, hepatic vein และ inferior vena cava (IVC) เพื่อประเมินระดับของ venous congestion
การตรวจเหล่านี้ใช้ในการพยากรณ์โรคและติดตามผลการรักษาในผู้ป่วย CRS ได้อย่างมีประสิทธิภาพ5
การรักษา6
- ยาขับปัสสาวะ (Diuretics)
การรักษาหลักคือการใช้ loop diuretics เช่น furosemide ซึ่งยับยั้งการดูดกลับของโซเดียมและน้ำที่ไต (รูปที่ 2) การให้แบบ intermittent เทียบกับ continuous dosing พบว่า decongestion และการทำงานของไตไม่แตกต่างกัน การใช้ยาขับปัสสาวะชนิดอื่นร่วมกัน (sequential nephron blockade) ช่วยลด congestion ได้มากขึ้น เช่น ADVOR trial7 เป็นการศึกษาในผู้ป่วย acute HF ที่มี eGFR >20 mL/min/1.73 m2 โดยเปรียบเทียบผลของการให้ acetazolamide 500 mg/day ทางหลอดเลือดดำ ร่วมกับ loop diuretics เทียบกับการให้ loop diuretics เพียงอย่างเดียว พบว่ากลุ่มที่ได้รับ acetazolamide ร่วมกับ loop diuretics ช่วยลด congestion ได้มากกว่า แต่อัตราการเสียชีวิตและ HF hospitalization ไม่แตกต่างกัน นอกจากนี้ EMPULSE trial8 พบว่าการให้ empagliflozin 10 mg/day ร่วมกับ loop diuretics ในผู้ป่วย acute HF ที่มี eGFR >20 mL/min/1.73 m2 ช่วยลดภาวะ congestion, อัตราการเสียชีวิต และ HF hospitalization ได้ ส่วน spironolactone ใช้เวลาในการออกฤทธิ์ 2-3 วัน จึงอาจไม่ช่วยลด congestion ได้ดีในภาวะ acute HF - Tolvaptan (V2 receptor antagonist)
Tolvaptan ออกฤทธิ์โดยการยับยั้ง V2 receptor ที่ collecting duct ของไต ทำให้เกิดการขับน้ำออก (aquaresis) และช่วยเพิ่มระดับโซเดียมในเลือดในผู้ป่วย hyponatremia ได้ โดย tolvaptan ช่วยลดภาวะ congestion ได้มากขึ้นภายใน 24-48 ชั่วโมง แต่ไม่ช่วยลดอัตราการเสียชีวิต ขนาดยาโดยทั่วไปคือ 15-30 mg/day - Ultrafiltration
เป็นกระบวนการขจัดน้ำส่วนเกินออกจากพลาสมา โดยการนำเลือดผ่านตัวกรองและใช้ negative pressure ดึงน้ำออก เมื่อเปรียบเทียบระหว่างการใช้ diuretics กับ ultrafiltration พบว่า ultrafiltration ช่วยลด congestion ได้มากกว่า อย่างไรก็ตาม พบอัตราการเกิด AKI สูงกว่าการใช้ diuretics ดังนั้นควรพิจารณาใช้เฉพาะในกรณีที่ไม่ตอบสนองต่อยาขับปัสสาวะ
 รูปที่ 2 แนวทางการให้ยาขับปัสสาวะในผู้ป่วย acute heart failure9
รูปที่ 2 แนวทางการให้ยาขับปัสสาวะในผู้ป่วย acute heart failure9
คำย่อ CO, cardiac output; HCTZ, hydrochlorothiazide, SR, sustained release
ข้อควรระวัง การใช้ urine sodium เพื่อประเมินการตอบสนองต่อ furosemide ควรใช้ภายใน 24-72 ชั่วโมงแรก เท่านั้น เนื่องจากหลังจากนั้นอาจมีข้อจำกัดในการแปลผล จากกระบวนการ renal tubular adaptation
ภาวะดื้อต่อยาขับปัสสาวะ (Diuretic resistance)10
- ภาวะไตวาย ส่งผลให้มีการสะสมของ organic anions ซึ่งไปแย่งจับกับ diuretic และลดการหลั่งของยาเข้าสู่ proximal tubule ทำให้ยาที่ไปออกฤทธิ์ที่ thick ascending limb ลดลง
- การได้รับยาบางชนิด เช่น NSAIDs ซึ่งแย่งจับกับ diuretic ในการถูกขับออกทาง proximal tubule ทำให้ประสิทธิภาพยาลดลง
- ภาวะโปรตีนในเลือดต่ำ หรือ มีการสูญเสียอัลบูมินทางปัสสาวะ ทำให้การออกฤทธิ์ของยาขับปัสสาวะลดลง
- Diuretic braking phenomenon เกิดจากการใช้ยาขับปัสสาวะต่อเนื่อง ส่งผลให้เกิด nephron remodeling และเพิ่มการดูดกลับโซเดียมและน้ำที่ไต อาจรักษาโดยเพิ่มขนาดของยาขับปัสสาวะ ใช้ยาขับปัสสาวะชนิดอื่นร่วมกัน หรือ ultrafiltration ในกรณีที่ไม่ตอบสนองต่อการรักษาด้วยยา
สรุป
Cardiorenal syndrome เป็นภาวะที่การทำงานของหัวใจหรือไตบกพร่อง ส่งผลกระทบซึ่งกันและกัน นำไปสู่การทำงานของอีกระบบหนึ่งที่แย่ลงตาม โดยสามารถจำแนกออกเป็น 5 ชนิด ตามพยาธิสรีรวิทยา ปัจจุบันมีการศึกษามากขึ้นเกี่ยวกับ biomarkers เพื่อช่วยในการวินิจฉัย ประเมินความเสี่ยง และพยากรณ์โรค โดยเฉพาะในผู้ป่วย Type 1 CRS แนวทางการรักษาหลักคือ decongestion ซึ่งได้แก่ การใช้ยาขับปัสสาวะ หรือในบางกรณีที่ดื้อต่อยา อาจพิจารณาใช้ ultrafiltration
- Banerjee D, Ali MA, Wang AYM, Jha V. Acute kidney injury in acute heart failure-when to worry and when not to worry? Nephrol Dial Transplant. 2024;40:10–8.
- Gallo G, Lanza O, Savoia C. New Insight in Cardiorenal Syndrome: From Biomarkers to Therapy. Int J Mol Sci. 2023;24:5089.
- Núñez J, de la Espriella R, Rossignol P, Voors AA, Mullens W, Metra M, et al. Congestion in heart failure: a circulating biomarker-based perspective. A review from the Biomarkers Working Group of the Heart Failure Association, European Society of Cardiology. Eur J Heart Fail. 2022;24:1751–66.
- Schanz M, Shi J, Wasser C, Alscher MD, Kimmel M. Urinary [TIMP-2] × [IGFBP7] for risk prediction of acute kidney injury in decompensated heart failure. Clin Cardiol. 2017;40:485–91.
- Beaubien-Souligny W, Rola P, Haycock K, Bouchard J, Lamarche Y, Spiegel R, et al. Quantifying systemic congestion with Point-Of-Care ultrasound: development of the venous excess ultrasound grading system. Ultrasound J. 2020;12:16.
- McCallum W, Sarnak MJ. Cardiorenal Syndrome in the Hospital. Clin J Am Soc Nephrol. 2023;18:933–45.
- Mullens W, Dauw J, Martens P, Verbrugge FH, Nijst P, Meekers E, et al. Acetazolamide in Acute Decompensated Heart Failure with Volume Overload. N Engl J Med. 2022;387:1185–95.
- Voors AA, Angermann CE, Teerlink JR, Collins SP, Kosiborod M, Biegus J, et al. The SGLT2 inhibitor empagliflozin in patients hospitalized for acute heart failure: a multinational randomized trial. Nat Med. 2022;28:568–74.
- Tran P, Khweir L, Kuehl M, Joshi M, Appunu K, Ayub W, et al. A Pragmatic Approach to Acute Cardiorenal Syndrome: Diagnostic Strategies and Targeted Therapies to Overcome Diuretic Resistance. J Clin Med. 2025;14:2996.
- Lo KB, Janakiraman A, Rangaswami J. Kidney Dysfunction in Heart Failure: Core Curriculum 2025. Am J Kidney Dis. 2025;86:109–24.





