 ศ. พญ. นฤชา จิรกาลวสาน
ศ. พญ. นฤชา จิรกาลวสาน
สาขาวิชาอายุรศาสตร์โรคระบบการหายใจและภาวะวิกฤต
ภาควิชาอายุรศาสตร์ คณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย
ศูนย์นิทราเวช รพ.จุฬาลงกรณ์ สภากาชาดไทย
บทนำ
การรักษาหลักของผู้ป่วยโรคหยุดหายใจขณะหลับจากการอุดกั้น (obstructive sleep apnea หรือ OSA) ซึ่งพบได้ถึงประมาณร้อยละ 14 ในประชากรทั่วไป1 คือ การใช้เครื่องอัดอากาศแรงดันบวก (continuous positive airway pressure) แต่อย่างไรก็ตามมีผู้ป่วยถึงร้อยละ 29 – 832 ที่ไม่สามารถทนต่อการรักษาด้วยวิธีนี้ได้ เมื่อประมาณกว่า 10 ปีที่ผ่าน มีการรักษาทางเลือกด้วยวิธีใหม่คือการใช้อุปกรณ์กระตุ้นเส้นประสาทสมองคู่ที่ 12 (hypoglossal nerve stimulation) โดยที่การรักษาด้วยวิธีนี้ผ่านการรับรองโดยองค์การอาหารและยาแห่งสหรัฐอเมริกา (Food and Drug Administration: FDA) เมื่อปี พ.ศ. 2557
โดยเส้นประสาทสมองคู่ที่ 12 (hypoglossal nerve) เป็นเส้นประสาทสมองที่ควบคุมการทำงานของกล้ามเนื้อ genioglossus ซึ่งเป็นกล้ามเนื้อสำคัญที่สุดที่ทำหน้าที่ขยายทางเดินหายใจส่วนบน เมื่อกล้ามเนื้อหดตัว จะทำให้ลิ้นเคลื่อนที่ไปด้านหน้า ทำให้มีพื้นที่ของ pharynx เพิ่มขึ้นทั้งในระดับ velum และ oropharynx ทำให้ทางเดินหายใจส่วนบนกว้างขึ้น และทำให้แรงดันที่จะกดทางเดินหายใจส่วนบน (critical pressure หรือ Pcrit) ลดลง1 โดยการผ่าตัดนี้เป็นการรักษาที่มุ่งนี้การรักษาผ่านทาง endotype กลุ่มของการตอบสนองของกล้ามเนื้อไม่ดี (poor muscle responsiveness)
โดยประโยชน์ของการกระตุ้นเส้นประสาท hypoglossal ที่มีต่อภาวะ OSA ถูกค้นพบครั้งแรกในปี ค.ศ. 1993 โดย Schwartz et al. ซึ่งพบว่าการกระตุ้นเส้นประสาท hypoglossal ในสัตว์ทดลอง สามารถทำให้ Pcrit ลดลง3 การศึกษาต่อมาในมนุษย์ พบว่าการกระตุ้นที่เส้นประสาท hypoglossal ในผู้ป่วย OSA สามารถลด apnea hypopnea index (AHI), oxygen desaturation index (ODI) และทำให้ลักษณะการหายใจที่มีลักษณะ inspiratory flow limitation ดีขึ้น4
โดยการกระตุ้นเส้นประสาท hypoglossal ด้วยอุปกรณ์ทางการแพทย์มีหลายแบบ โดยสามารถเรียกรวมว่าเป็นการักษาโดยการกระตุ้นกล้ามเนื้อทางเดินหายใจส่วนบน (upper airway stimulation หรือ UAS) โดยขณะนี้มีเพียงอุปกรณ์ชนิดเดียวที่เข้าประเทศไทย คือ hypoglossal nerve stimulation โดยบริษัท Inspire Medical Systems, Inc, Maple Grove, MN
โดยขณะนี้ประเทศไทยสามารถให้การรักษาด้วยวิธีนี้ได้เป็นลำดับที่ 4 ในเอเชีย หลังจากประเทศญี่ปุ่น ประเทศสิงคโปร์ และฮ่องกง โดยที่ประเทศไทยมีการผ่าตัดเป็นครั้งแรกที่โรงพยาบาลจุฬาลงกรณ์ สภากาชาดไทย ปัจจุบันอุปกรณ์ดังกล่าวที่ผ่านการรับรองจากองค์การอาหารและยาแห่งประเทศไทย (อ.ย.) เมื่อปี พ.ศ. 2567
ข้อบ่งชี้
ปกติจะพิจารณาการรักษาด้วยวิธี UAS ในผู้ป่วย OSA ระดับปานกลางถึงรุนแรง ที่ไม่สามารถใช้ CPAP หรือปฏิเสธการใช้ CPAP มีการศึกษาพบว่า ผลสำเร็จของการผ่าตัดจะดีขึ้นที่ดัชนีมวลกายไม่เกิน 32 กก./ม2 และ AHI ไม่เกิน 505 อย่างไรก็ตามล่าสุด ได้มีการปรับเกณฑ์ดัชนีมวยกายไปถึง 40 กก./ม2 และ AHI ไปถึง 1006 นอกจากนั้นผู้ป่วยควรได้รับการทำ drug-induced sleep endoscopy โดยหากใช้ VOTE classification7 ผู้ป่วยไม่ควรมีลักษณะ complete concentric collapse ที่ระดับ velum เนื่องจาก มีความสัมพันธ์กับโอกาสต่ำที่จะประสบผลสำเร็จจากการผ่าตัด รวมทั้งไม่ควรมีค่า central AHI และ mixed AHI มากกว่าร้อยละ 25
การติดตั้งอุปกรณ์ UAS8
อุปกรณ์จะทำงานโดยการกระตุ้นเส้นประสาท hypoglossal เพื่อขยายพื้นที่ของทางเดินหายใจส่วนบน โดยอุปกรณ์ทั้งหมดจะติดตั้งไว้ที่ด้านขวา โดยอุปกรณ์จะประกอบไปด้วย 3 ส่วน (รูปที่ 1) คือ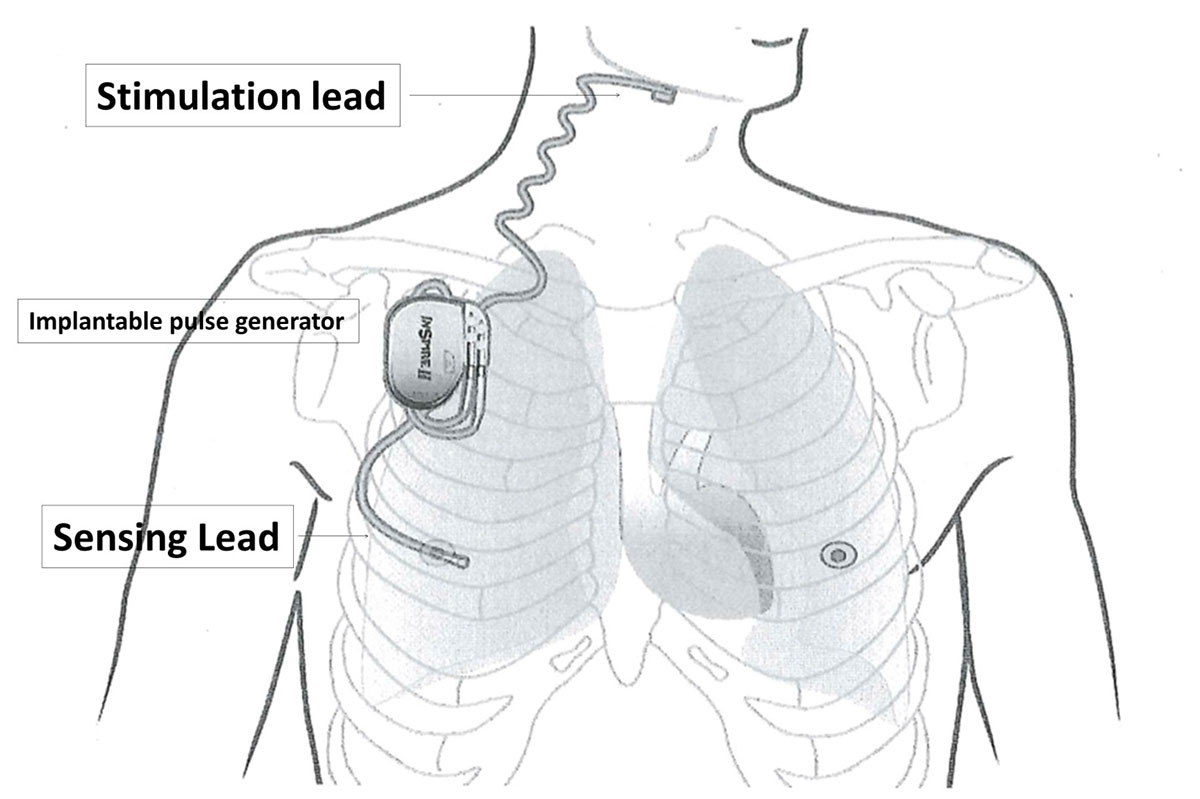 รูปที่ 1 อุปกรณ์ hypoglossal nerve stimulation (Inspire Medical Systems)
รูปที่ 1 อุปกรณ์ hypoglossal nerve stimulation (Inspire Medical Systems)
- Sensing lead โดยอุปกรณ์ส่วนนี้ทำหน้าที่รับสัญญาณว่าเริ่มมีการหายใจเข้าเกิดขึ้น โดยอุปกรณ์นี้จะติดตั้งไว้ที่ intercostal space ที่ 4 – 6 ระหว่างกล้ามเนื้อ internal และ external intercostal
- Implantable pulse generator โดยอุปกรณ์นี้จะทำหน้าที่รับข้อมูลจังหวะการหายใจจาก sensing lead และส่งสัญญาณต่อไปยัง stimulation lead ให้สอดคล้องกับจังหวะการหายใจ อุปกรณ์นี้จะติดตั้งไว้ที่ชั้นใต้ผิวหนัง ในตำแหน่ง infraclavicular และเหนือต่อ fascia ของกล้ามเนื้อ pectoralis major
- Stimulation lead โดยอุปกรณ์จะทำหน้าที่ส่งสัญญาณไฟฟ้าไปกระตุ้นเส้นประสาท hypoglossal ซึ่งจะกระตุ้นกล้ามเนื้อ genioglossus ให้หดตัว ทำให้ลิ้นยื่นไปด้านหน้า จึงทำให้ทางเดินหายใจกว้างขึ้น อุปกรณ์ชิ้นนี้จะคล้องไว้กับเส้นประสาท hypoglossal ด้านขวาโดยตรง
ระยะเวลาในการผ่าตัดเพื่อติดตั้งอุปกรณ์นี้ใช้เวลาเฉลี่ยประมาณ 140 นาที โดยผู้ป่วยส่วนใหญ่จำเป็นต้องพักฟื้นที่โรงพยาบาลเพียง 1 คืนหลังผ่าตัด เครื่อง UAS จะถูกเปิด ที่ประมาณ 1 เดือนหลังผ่าตัด และผู้ป่วยจะได้รับการตรวจการนอนหลับเพื่อปรับเครื่อง (titration) เพื่อให้การกระตุ้นเส้นประสาท hypoglossal เข้ากับจังหวะการหายใจ และเพียงพอที่จะรักษาภาวะ OSA ของผู้ป่วย
ประสิทธิภาพในการรักษา OSA
UAS มีประสิทธิภาพในการรักษา OSA ในระยะยาว และประสิทธิภาพจะคงอยู่ตราบที่ได้เปิดใช้เครื่อง จากการติดตามผลการรักษาเป็นระยะเวลา 12 เดือน การใช้เครื่อง UAS ในกลุ่มที่เป็น OSA ระดับปานกลางถึงรุนแรง (ที่มีข้อบ่งชี้โดยผู้ป่วยมีลักษณะที่เอื้อต่อผลสำเร็จ เช่น AHI 20-50 และ ดัชนีมวลกาย ไม่เกิน 32 กิโลกรัมต่อตารางเมตร) และไม่มีลักษณะ complete concentric collapse ที่ระดับ velum จากการทำ DISE พบว่าเมื่อเปิดใช้ UAS ต่อเนื่อง เป็นระยะเวลานาน 12 เดือน จะทำให้ AHI ลดลงร้อยละ 68 จากตอนก่อนใช้ โดยมี median AHI ลดลงจาก 29.3 ครั้งต่อชั่วโมง เหลือ 9 ครั้งต่อชั่วโมง นอกจากนี้ ยังทำให้ ระยะเวลานอนหลับยาวนานขึ้น ความง่วงนอนช่วงกลางวันลดลง และคุณภาพชีวิตดีขึ้น อย่างมีนัยสำคัญ9
โดยมีข้อมูลที่ติดตามผู้ป่วยเป็นระยะเวลา 5 ปีพบว่าเครื่องยังคงมีประสิทธิภาพที่ดีในการรักษาภาวะหยุดหายใจณะหลับจากการอุดกั้น10
การเปิดใช้เครื่อง UAS ทำให้พื้นที่ของทางเดินหายใจส่วน retropalatal และ retrolingual กว้างขึ้นในขณะที่ทำ DISE เมื่อเทียบกับช่วงที่ไม่ได้เปิดเครื่อง โดยพื้นที่ส่วน retropalatal ขยายถึงร้อยละ 180 ในแนวหน้า-หลัง และ retrolingual ขยายถึงร้อยละ 130 โดยขยายในแนวทั้งหน้า-หลัง และด้านข้าง11
อย่างไรก็ตามแบตเตอรี่ของเครื่องจะมีอายุอยู่ที่ประมาณ 10 ปี ทำให้ทุก 10 ปี ต้องมีการผ่าตัดเพื่อเปลี่ยนแบตเตอรี่
ภาวะแทรกซ้อน
ภาวะแทรกซ้อนที่พบส่วนใหญ่มักไม่รุนแรง โดยรายงานที่พบส่วนมากจะเกี่ยวข้องกับความเจ็บ คืออาการเจ็บคอจากการใส่ท่อช่วยหายใจขณะผ่าตัด อาการปวดแผลผ่าตัด มีอาการเจ็บที่ลิ้น ขณะที่เปิดเครื่อง และพบรายงานเรื่องมีลิ้นเป็นอัมพาตชั่วคราวหลังผ่าตัดได้ร้อยละ 18 ซึ่งอาการทั้งหมดสามารถกลับมาเป็นปกติได้ในไม่กี่สัปดาห์ มีรายงานเครื่องหลุดเลื่อนจากตำแหน่งเดิม ทำให้ต้องกลับเข้าไปในห้องผ่าตัดเพื่อจัดตำแหน่งใหม่ และไม่พบรายงานการเสียชีวิตที่เกี่ยวข้องกับการผ่าตัดติดตั้งหรือการใช้เครื่อง9
สรุป
UAS จัดว่าเป็นการรักษาทางเลือกแบบหนึ่งของผู้ป่วยที่เป็น OSA ระดับปานกลางถึงรุนแรง ซึ่งมีผลลัพธ์น่าพอใจ และภาวะแทรกซ้อนหลังผ่าตัดน้อย และขณะประเทศไทยได้มีการรักษาด้วยวิธีนี้แล้ว
- Oliven A, Tov N, Geitini L, Steinfeld U, Oliven R, Schwartz AR, et al. Effect of genioglossus contraction on pharyngeal lumen and airflow in sleep apnoea patients. Eur Respir J. 2007;30(4):748-58.
- Weaver TE, Grunstein RR. Adherence to continuous positive airway pressure therapy: the challenge to effective treatment. Proc Am Thorac Soc. 2008;5:173–8.
- Schwartz AR, Thut DC, Russ B, Seelagy M, Yuan X, Brower RG, et al. Effect of electrical stimulation of the hypoglossal nerve on airflow mechanics in the isolated upper airway. Am Rev Respir Dis. 1993;147(5):1144-50.
- Schwartz AR, Bennett ML, Smith PL, De Backer W, Hedner J, Boudewyns A, et al. Therapeutic electrical stimulation of the hypoglossal nerve in obstructive sleep apnea. Arch Otolaryngol Head Neck Surg. 2001;127(10):1216-23.
- Van de Heyning PH, Badr MS, Baskin JZ, Cramer Bornemann MA, De Backer WA, Dotan Y et al. Implanted upper airway stimulation device for obstructive sleep apnea. Laryngoscope. 2012;122(7):1626-33.
- https://www.fda.gov/medical-devices/recently-approved-devices/inspire-upper-airway-stimulation-p130008s090
- Kezirian EJ, Hohenhorst W, de Vries N. Drug-induced sleep endoscopy: the VOTE classification. Eur Arch Otorhinolaryngol. 2011;268(8):1233-6.
- Maurer JT, Van de Heyning P, Lin H-S, Baskin J, Anders C, Hohenhorst W, et al. Operative technique of upper airway stimulation: an implantable treatment of obstructive sleep apnea. Oper Tech Otolayngol Head Neck Surg.2012;23(3):227-33.
- Strollo PJ, Jr., Soose RJ, Maurer JT, de Vries N, Cornelius J, Froymovich O, et al. Upper-airway stimulation for obstructive sleep apnea. N Engl J Med. 2014;370(2):139-49.
- Woodson BT, Strohl KP, Soose RJ, Gillespie MB, Maurer JT, de Vries N, et al. Upper Airway Stimulation for Obstructive Sleep Apnea: 5-Year Outcomes. Otolaryngol Head Neck Surg. 2018;159(1):194-202.
- Safiruddin F, Vanderveken OM, de Vries N, Maurer JT, Lee K, Ni Q, et al. Effect of upper-airway stimulation for obstructive sleep apnoea on airway dimensions. Eur Respir J. 2015;45(1):129-38.





